Классификация панкреатита по узи

Журнал “SonoAce Ultrasound”
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Введение
В России за последние годы отмечена тенденция к увеличению количества больных острым панкреатитом, частота которого достигает 2,5 – 8,4% среди пациентов с острыми хирургическими заболеваниями органов брюшной полости [1]. В странах Западной Европы, в частности, в Дании с 1979 по 1992 гг., частота острого панкреатита увеличилась с 26,8 до 35,4 на 100000 населения [15], т.е. на 25%. По данным М. В. Гринева [8], из всех больных с острым панкреатитом деструктивные формы отмечены у 16,2%, которые при прогрессировании приводят к летальности почти в 50% случаев [4].
Благодаря новым методам исследования (УЗИ, КТР, ЯМР) улучшилась ранняя диагностика острого панкреатита и его осложнений, появилась возможность динамического наблюдения за больными в процессе лечения. Для широкой практики особый интерес представляет ультразвуковая диагностика – неинвазивный, неионизирующий метод, который можно применять многократно, не причиняя вреда больному. С помощью эхографии стало возможным эффективно проводить не только диагностические, но и лечебные малоинвазивные вмешательства на поджелудочной железе – биопсию, дренирование патологических образований и т.д. [4, 6, 8].
Несмотря на интенсивное внедрение эхографии в практику и определенные успехи в изучении возможностей метода, в литературе еще недостаточно освещены вопросы, касающиеся деталей ультразвуковой семиотики острого панкреатита. Не конкретизирована эхографическая картина острого панкреатита в зависимости от стадии заболевания, мало отражены вопросы, касающиеся диагностики осложнений острого панкреатита, особенно редких, но клинически значимых [2, 5, 9 – 14, 16]. У пациентов, лечившихся оперативно по поводу острого панкреатита, актуальной остается проблема ультразвукового мониторинга в послеоперационном периоде. Практически не изучена роль данных ультразвукового исследования для выработки индивидуальной тактики лечения и прогнозирования возможных осложнений у каждого конкретного больного.
Материалы и методы
В основу работы положены данные 534 УЗ-исследований у 278 пациентов с острым панкреатитом, находившихся на лечении в городской клинической больнице N 9 за период 1992-1995 гг. Исследования проводились с помощью ультразвукового сканера, оснащенного конвексным датчиком 3,5 МГц и секторным – 5 МГц.
Результаты
На основе наших наблюдений выявлены следующие сонографические особенности острого панкреатита:
Изменения непосредственно в поджелудочной железе:
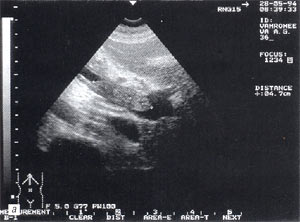
- увеличение размеров поджелудочной железы (рис. 1) – отмечено в 88% случаев. Нормальные размеры поджелудочной железы: головка 3-4,5 см; тело 2,5 – 3 см; хвост 3-4 см;
- нечеткость контуров – 90,6% случаев;
- увеличение расстояния между задней стенкой желудка и передней поверхностью поджелудочной железы свыше 3 мм и достигающее 10 – 20 мм, что характеризует отек парапанкреатических тканей, отмечено в 53% наблюдений (рис. 1);
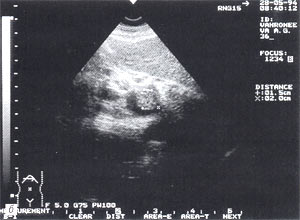
- изменение эхогенности железы: повышение – 85,6% случаев (рис. 2); нормальная – 8,6% случаев; понижение – 5,8% случаев.
Рис. 1. Острый панкреатит, деструктивная форма. Увеличение размеров поджелудочной железы, нечеткость контуров, увеличение расстояния между задней стенкой желудка и поджелудочной железы.
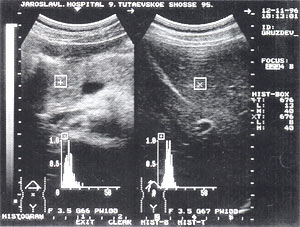
Рис. 2. Острый панкреатит, повышение эхогенности поджелудочной железы (по сравнению с эхогенностью печени).
Изменения в брюшной полости, являющиеся косвенными признаками острого панкреатита и относящиеся к его осложнениям:
Оментобурсит (рис. 3) встречается в 28,4% случаев (из них 48% у мужчин и 52% у женщин). Некоторые авторы обозначают эту патологию как “псевдокиста поджелудочной железы”. Отмечен объем таких образований от 5мл (малые объемы необходимо дифференцировать с сосудистыми аневризмами) до 3 л и более. Скорость формирования оментобурсита при остром панкреатите от 2 – 4 дн. от начала заболевания до 2 – 4 нед. При ультразвуковом исследовании оментобурсит представлен в виде анэхогенного образования с четкими контурами, неправильной или округлой формы, чаще с однородной структурой, с толщиной стенок 0,2 – 0,4 см. При эхографическом мониторинге утолщение стенки до 0,5 – 1,0 см с появлением неоднородности структуры следует расценивать как сонографический признак абсцедирования.
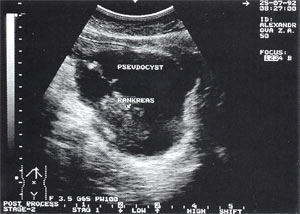
Рис. 3. Псевдокиста поджелудочной железы при остром панкреатите в виде анэхогенного образования с четкими контурами, однородной структурой, с наличием гиперэхогенных включений (детрит поджелудочной железы).
Свободная жидкость в брюшной полости – отмечена в 18% случаев (рис. 4), из них 80% у мужчин и 20% у женщин. Жидкость в объеме до 100 мл определяется только в одной анатомической области ( чаще в малом тазу), более 100 мл – по боковым каналам и в других отделах брюшной полости. В первые дни развития острого панкреатита жидкость гомогенная, после 6-12 сут. часто структура неоднородная из-за “нитевидных” включений (как правило, фибрин).
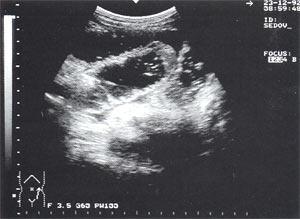
Рис. 4. Расширенные петли тонкого кишечника до 3,5 см, заполненные жидким содержимым на фоне свободной жидкости в брюшной полости.
Билиарная гипертензия – встречается в 13% случаев, из них 25% у мужчин и 75% у женщин. При эхографии отмечается расширение внутрипеченочных желчных протоков, общего печеночного протока и общего желчного протока. При отсутствии холедохолитиаза билиарная гипертензия как правило наблюдается при очаговом панкреонекрозе в области головки поджелудочной железы.
Инфильтраты брюшной полости – обнаруживаются в 5,4% случаев (рис. 5, 6), в том числе 64% у мужчин и 36% у женщин. Как правило, инфильтрируется большой сальник (оментит), визуализирующийся в виде образования повышенной эхогенности с нечеткими неровными контурами, неоднородной структурой, с участками пониженной эхогенности, которые могут свидетельствовать о формировании в нем абсцессов. Размеры инфильтратов от 5 до 15 – 20 см.
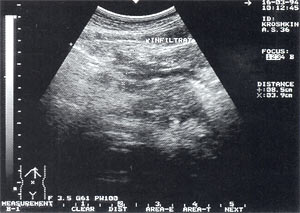
Рис. 5. Инфильтрат в брюшной полости в проекции большого сальника – представлен образованием неправильной формы с нечеткими контурами, неоднородной структурой, с наличием гипер- и гипоэхогенных участков. Размер инфильтрата 8,5 х 3,9 х 5,3см.
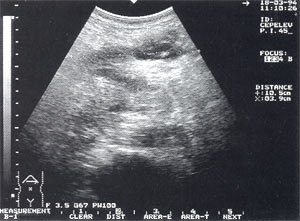
Рис. 6. Инфильтрат в проекции большого сальника с анэхогенным включением до 4 см (абсцедирование).
Забрюшинные флегмоны – встречаются в 4,3% случаев (рис. 7), из них 67% у мужчин и 33% у женщин. В 95% случаев диагностирована левосторонняя локализация флегмоны, которая определялась в виде анэхогенного или гипоэхогенного образования чаще щелевидной или овальной формы. Как правило, причиной развития данного осложнения является распространение панкреатического секрета по забрюшинному пространству из псевдокисты, иногда доходящее до паховой области. Панкреатогенный паранефрит можно рассматривать как вариант забрюшинной флегмоны.
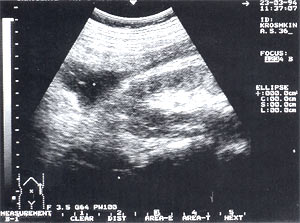
Рис. 7. Забрюшинная флегмона слева – анэхогенное образование неправильной формы с нечеткими контурами. Сканирование проведено из левой поясничной области.
Гидроторакс – встречается в 2,2% случаев, одинаково часто у мужчин и женщин, с преимущественно левосторонней локализацией.
Тромбоз в системе воротной вены – отмечается в 1,5% случаев (рис. 8 а, б) и достаточно хорошо может быть определен, по нашему мнению, без допплеровского исследования. При признаках портальной гипертензии обязательно должно выполняться прицельное ультразвуковое исследование сосудов системы воротной вены. Тромбы могут быть одиночными и множественными. Они локализуются как в самой воротной вене, так и в селезеночной и верхнебрыжеечной венах.
Рис. 8. Тромбоз воротной вены. Просвет вены полностью обтурирован изоэхогенным образованием с четкими контурами, неоднородной структурой, длиной до 4,7 см (а – cагиттальный срез, б – поперечный срез).
Парез кишечника – встречается в 1,4% случаев (см. рис. 4), из них 75% у мужчин и 25% у женщин. Характеризуется расширением петель тонкого кишечника до 3 – 5 см с заполнением их жидким содержимым и регистрируемой “маятникообразной” перистальтикой.
Гидроперикард – встречается в 0,4% случаев.
Восходящий медиастенит, отмечаемый другими авторами, нами не наблюдался.
Абсцессы поджелудочной железы – встречаются как правило на фоне уже имеющихся ультразвуковых признаков хронического панкреатита.
Разрывы псевдокист поджелудочной железы при ультразвуковой диагностике наблюдались у 2 больных (0,7%).
Кровоизлияние в псевдокисту поджелудочной железы с формированием организованной гематомы (рис. 9) отмечено у 1 пациента (0,35%).
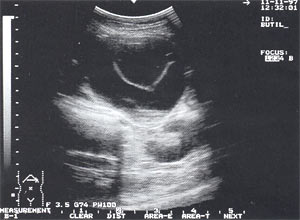
Рис. 9. Псевдокиста поджелудочной железы в виде анэхогенного образования с четкими контурами, в котором определяется другое анэхогенное образование с капсулой 0,2 – 0,3 см (на операции – псевдокиста с организовавшейся гематомой).
Псевдокисты поджелудочной железы с атипичной локализацией (в печени, селезенке, перидуоденально и т.д.) выявлены у 2 больных – 0,7% (рис. 10).
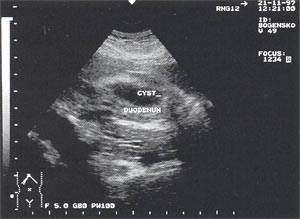
Рис. 10. Атипично расположенная псевдокиста поджелудочной железы (парадуоденально) в виде анэхогенного образования округлой формы с четкими контурами, однородной структурой, размером до 4,5 см, расположенного рядом с двенадцатиперстной кишкой.
Инфаркты селезенки (1 больная – 0,35%) – на фоне тромбоза воротной вены с портальной гипертензией.
Разрывы селезенки вследствие портальной гипертензии (нами не наблюдались).
Панкреатогенные паранефриты – обнаружены у 2 пациентов, что составило 0,7% (рис. 11).
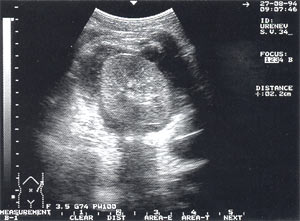
Рис. 11. Левосторонний панкреатогенный паранефрит, визуализирующийся в виде жидкостного образования, окружающего почку со всех сторон. Поперечный срез.
Заключение
Проведенное исследование показывает, что ультразвуковая диагностика должна быть обязательным элементом диагностического алгоритма у больных острым панкреатитом. Для повышения диагностической ценности эхографии необходима определенная последовательность в выполнении ультразвукового исследования: детальный осмотр парапанкреатических тканей и самой железы; осмотр всех отделов брюшной полости на предмет свободной жидкости и инфильтратов; осмотр плевральных полостей и полости перикарда на наличие выпота; детальный осмотр внутри- и внепеченочных желчных протоков; прицельный осмотр сосудов системы воротной вены; исследование забрюшинного пространства; динамическое наблюдение (частота повторного УЗИ определяется степенью тяжести заболевания и вероятностью развития осложнений).
Для улучшения получаемых результатов УЗИ могут быть рекомендованы следующие технические приемы:
- при плохой визуализации хвост поджелудочной железы лучше исследовать через селезенку или левую почку;
- для улучшения визуализации поджелудочной железы можно применять заполнение желудка 500 – 800 мл дегазированной жидкости (воды);
- использовать датчики с различной частотой излучения для более детального исследования патологических очагов, расположенных на разном расстоянии от датчика;
- использовать полипозиционное сканирование с дозированной компрессией на брюшную стенку для улучшения визуализации исследуемых органов, что позволяет “раздвигать” петли кишечника, создавая тем самым дополнительное “акустическое окно”;
- применять ультразвуковую фистулографию с жидкими и газообразующими растворами (фурацилин, новокаин, “Echovist”) для определения полостей при наличии панкреатических свищей [7], что может быть предметом отдельных исследований.
Литература
- Скуя Н. А. Заболевания поджелудочной железы. – М.: Медицина, 1986.
- Зубарев А. Р., Григорян Р. А. Ультразвуковое ангиосканирование. – М.: Медицина, 1990.
- Филин В. И., Костюченко А. А.. Неотложная панкреатология. – СПб., 1994.
- Нестеренко Ю. А., Михайлусов С. В., Иманалиев М. Р. Ультразвук в диагностике и лечении панкреонекроза/ Сб. научн. тр. Пленума проблемной комиссии по неотложной хирургии. – М.: 1994. – С. 26 – 29.
- Баранов Г. А., Могутов М. С, Завьялова Н. И. Ультразвуковая диагностика тромбоза воротной вены как редкого осложнения острого панкреатита/ Сб. науч. тр. международной конференции “Новые технологии в диагностике и в хирургии органов билиопанкреатодуоденальной зоны”. – М.: 1995. – С. 4 – 5.
- Белокуров ГО. Я., Уткин А. К., Жохов В. К., Белокуров С. Ю., Могутов М. С. Предпосылки использования прецизионной техники в лечении ложных кист поджелудочной железы/ Сб. научн. тр. международной конференции “Новые технологии в диагностике и в хирургии органов билиопанкреатодуоденальной зоны”. М.: 1995. – С. 78.
- Буйлов В. М., Могутов М. С, Карпов Н. Р. Ультразвуковая фистулография с “Echovist-300” в хирургии и урологии. – Материалы II съезда Ассоциации специалистов ультразвуковой диагностики в медицине. – М.: 1995. – С. 80.
- Гринев М. В., Красногоров В. Б., Рысс А. С, Веселов В. С, Смелянский А. И., Алексеенко Е. Н. Эффективная тактика лечения деструктивного панкреатита на основе раннего плазмафереза и малоинвазивных хирургических вмешательств/ Сб. научн. тр. “Малоинвазивные вмешательства в хирургии”. М.: 1996. – С. 257.
- McCormick P. A., Chronos N., Burroughs A. К., Mclntyre N., McLaughlinJ.E. Pancreatic pseudocyst causing portal vein thrombosis and pancreatico – pleural fistula.In: Gut (1990 May) 31(5):561-3.
- Fernandez-Cruz-L., Margarona-E., Llovera-J., Lopez-Boado-M. A., Saenz-HT. Pancreatic ascites. Hepatogastroenterology. 1993 Apr; 40(2): 150-4.
- Nishida-K., Terai-Y., Nojiri-L, Kato-M., Higashijima-M., Takagi-K., Adashi-R. A case of pancreatic pseudocyst with intracystic hemorrhage and repeated gastrointestinal bleeding. Nippon-Ronen-Igakkai-Zasshi. 1993 Aug; 30(8): 714-9.
- Sonak-R., Stock-W., Janzik-U., Hayduk-K., Borchard-F. Duodenal duplication cyst – a rare cause of acute recurrent pancreatitis. Leber-Magen-Darm. 1993 Sep; 23(5): 211-5.
- De-Ronde-T., Van-Beers-B., de-Canniere-L., Trigaux-JP., Melange-M. Thrombosis of splenic artery pseudoaneurysm complicating pancreatitis. Gut. 1993 Sep; 34(9): 1271-3.
- Hamm-B., Franzen-N. Atypically located pancreatic pseudocysts in the liver, spleen, stomach wall and mediastinum: their CT diagnosis. Rofo-Fortschr-Geb-Rontgenstr-Neuen-Bildgeb-Verfahr. 1993 Dec; 159(6): 522-7.
- Worning-H. Acute pancreatitis in Denmark. Ugeskr-Laeger. 1994 Apr 4; 156(14): 2086-9.
- Yasuda I., Tomita E., Nishigaki Y., Ino Y., Shimizu H., Yamada T., Kawamura H., Kuroda T., Takahashi T., Nagura K. A case of portal vein thrombosis subsequent to acute pancreatitis. Nippon Shokakibyo Gakkai Zasshi (1995 Apr) 92(4):820-5.

Журнал “SonoAce Ultrasound”
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Источник

Атлантская классификация острого панкреатита (ОП) — это международная мультидисциплинарная классификация тяжести острого панкреатита. Она является результатом работы международной группы экспертов и была представлена в 1992 году на международном симпозиуме в Атланте, США, а в 2012 году была пересмотрена. Эта классификация опирается на патоморфологические особенности разных типов острого панкреатита с учетом длительности его течения.
Согласно Атлантской классификации, чтобы поставить диагноз ОП, требуется наличие двух из следующих трех признаков:
- характерная абдоминальная боль (постоянная сильная эпигастральная боль, часто с иррадиацией в спину, с острым началом);
- показатели сывороточной липазы (амилазы) по крайней мере в 3 раза выше верхней границы нормы;
- характерные признаки ОП при КТ с контрастным усилением либо, реже, магнитно-резонансной томографии (МРТ) или трансабдоминальном УЗИ.
То есть, если диагноз острого панкреатита установлен на основании клинической картины и повышения уровня активности ферментов, необязательно немедленно проводить лучевую диагностику для его подтверждения.
АК выделяет следующие морфологические типы ОП:
- интерстициальный отечный панкреатит
- некротизирующий панкреатит, который, в свою очередь, подразделяют на:
- панкреатический паренхиматозный некроз
- перипанкреатический некроз
- панкреатический паренхиматозный некроз в сочетании с перипанкреатическим некрозом (наиболее часто встречаемый)
Все типы некротизирующего панкреатита могут быть стерильными или инфицированными; главным признаком, указывающим на инфицированность при доступных методах визуализации является образование пузырьков газа.
Для определения тяжести процесса нужно учесть наличие местных и общих осложнений.
Местные осложнения:
- острое перипанкреатическое скопление жидкости;
- панкреатическая псевдокиста;
- острое некротическое скопление и отграниченный некроз; а также
- нарушение эвакуации из желудка, тромбоз селезеночной и воротной вен и некроз ободочной кишки;
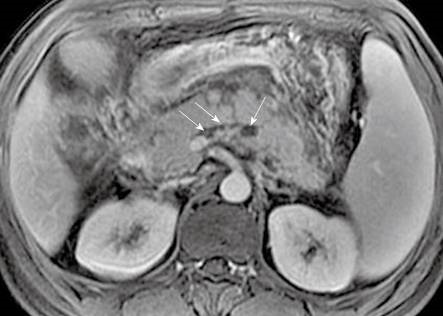
Рисунок 1 | Острый панкреатит, осложнившийся тромбозом селезеночной вены у мужчины 30 лет.
На аксиальной постконтрастной Т1ВИ можно увидеть дефекты наполнения в вовлеченных в процесс участках селезеночной вены (стрелки).
Определение как морфологического типа, так и местных осложнений во многом опирается на данные лучевых методов — и о них мы поговорим подробнее ниже.
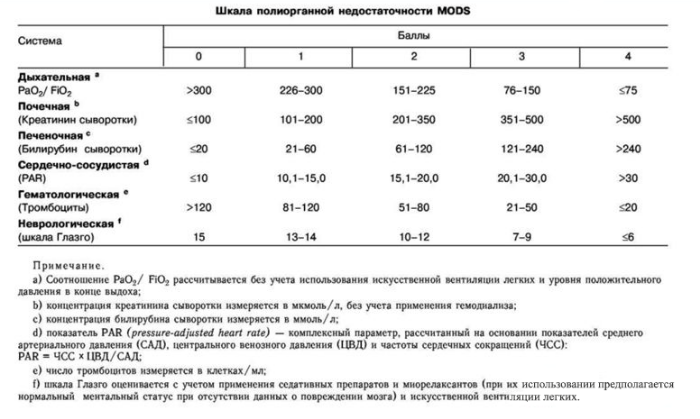
Общими осложнениями называют явления полиорганной недостаточности, которые могут быть переходящими (т. е. разрешаться в течение 48 часов) либо хроническими. Обострение уже существовавших сопутствующих заболеваний, таких как ишемическая болезнь сердца (ИБС), хронические заболевания легких, развившиеся вследствие ОП, также определяется как системное осложнение. Для определения органной недостаточности должны быть оценены три системы органов: дыхательная, сердечно-сосудистая и почечная. С этой целью используется модифицированная шкала Marshall (Табл. 1). Если имеется 2 и более баллов по данной шкале — присутствует органная недостаточность.
Таблица 1 | Шкала Marshall
По степени тяжести острый панкреатит (ОП) делится на легкий, средней тяжести и тяжелый.
- легкий ОП — нет признаков органной недостаточности, локальных или системных осложнений.
- средней тяжести ОП — признаки органной недостаточности, которая разрешается в течение 48 часов (преходящая органная недостаточность) и/или локальных или системных осложнений без продолжающейся органной недостаточности.
- тяжелый ОП — продолжающаяся более 48 часов органная недостаточность. Развитие инфицированного некроза у пациентов с продолжающейся органной недостаточностью связано с крайне высокой смертностью.
Поговорим о том, что представляют собой разные морфологические типы острого панкреатита и как они выглядят при лучевом исследовании.
Сразу оговоримся, что методом выбора в данном случае является КТ с контрастированием; УЗИ — зачастую менее информативный метод. МРТ выполняется реже из-за дороговизны и меньшей доступности метода, но может быть назначена в случае наличия противопоказаний к КТ (детский возраст, беременность, аллергические реакции на ионные контрастные вещества).
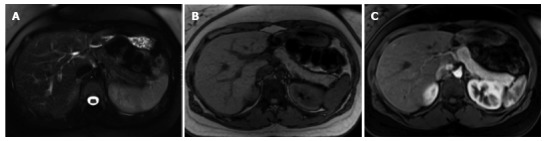
Рисунок 2 | Нормальная картина поджелудочной железы.
Т2ВИ с подавлением сигнала от жира (А) и GRE out-of-phase Т1ВИ (В) и постконтрастные Т1ВИ (С) в портовенозную фазу контрастирования.
Интерстициальный отечный панкреатит
Является воспалением паренхимы ПЖ и перипанкреатических тканей, но без видимых признаков тканевого некроза.
При КТ проявляется диффузным (редко — локальным) увеличением ПЖ в размерах, с гомогенным среднеинтенсивным накоплением контрастного вещества. Перипанкреатическая жировая клетчатка может выглядеть слегка «замутненной» или демонстрировать легкую тяжистость.
УЗИ-признаками являются увеличение размеров и гипоэхогенность ткани железы.
На МР-томограммах в Т1 взвешенных изображениях хорошо заметны увеличение размеров железы и размытость ее внешних границ; Т2-взвешенные томограммы (особенно с подавлением сигнала от жира) очень чувствительны и демонстрируют усиление сигнала от отечной ткани. Накопление контраста также гомогенное, может быть слегка пониженным в сравнении с картиной неизмененной поджелудочной железы.
Магнитно-резонансная холангиопанкреатография (МРХПГ) является крайне ценным методом для диагностики билиарного панкреатита: желчные конкременты четко визуализируются в виде участков «выпадения» сигнала.
Некротизирующий панкреатит
Процесс некроза, который может вовлекать либо ткань ПЖ и перипанкретические ткани, либо только перипанкертическую ткань, либо, реже всего, только паренхиму ПЖ.
Основной симптом некроза при КТ и МРТ с внутривенным контрастированием — область нарушения перфузии, т. е. зона, не накапливающая контрастное вещество; в первые недели эта область может выглядеть гетерогенно накапливающей контрастный препарат, а по прошествии времени (как правило, около недели) от начала симптомов формируются отграниченные области, которые явно не демонстрируют контрастного усиления.
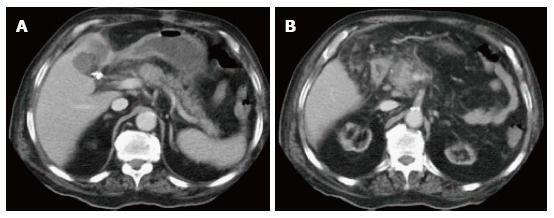
Рисунок 3
На аксиальных КТ-сканах в портовенозную фазу на уровне головки поджелудочной железы определяется участок нарушения перфузии, который не распространяется за пределы железы.
Лучше всего оценивать эти изменения на артериальной фазе контрастирования (наиболее ярко разница заметна в поздней артериальной и портовенозной фазах, когда неизмененная ткань ПЖ накапливает контрастный агент особенно интенсивно. Поздняя артериальная фаза (при КТ) наступает через 30–35 секунд после инъекционного или 15–20 секунд после болюсного введения контрастного препарата; должно определяться интенсивное контрастное усиление артерий и паренхимы органа; может также определяться незначительное количество контраста в портальной вене (из-за чего эта фаза также называется ранней портовенозной).
Обнаруженную по прошествии недели от начала симптомов область ткани ПЖ без контрастного усиления следует считать некрозом.
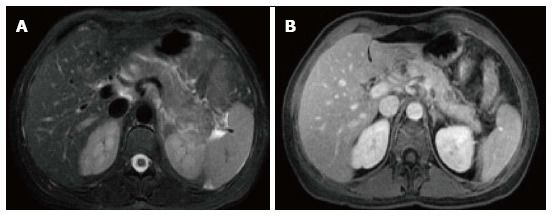
Рисунок 4 | Аксиальные спин-эхо Т2ВИ с подавлением сигнала от жира (А) и GRE Т1ВИ в портовенозную фазу контрастирования (В).
В проксимальной части хвоста железы определяется участок низкого Т2 сигнала, который демонстрирует снижение накопления контрастного препарата. Также можно увидеть тяжистость окружающей жировой клетчатки.
При развитии изолированного перипанкреатического некроза сама ткань ПЖ может выглядеть так же, как при интерстициальном панкреатите.
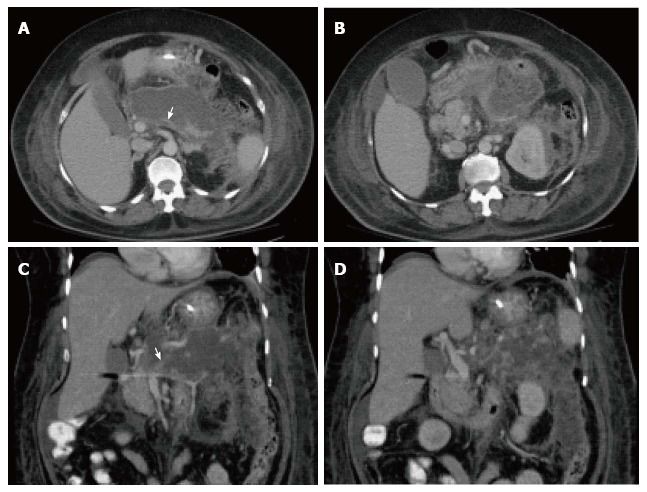
Рисунок 5 | Аксиальные (А, В) КТ-сканы в позднюю артериальную фазу контрастирования и их корональные (С, D) реконструкции.
Тело и хвост поджелудочной железы не накапливают контрастный препарат (полностью замещены некрозом). Гетерогенная область некроза и воспаления перипанкреатической жировой клетчатки. Стрелка указывает на тромбированную селезеночную вену (локальное осложнение процесса).
УЗИ:
При ОП одним из наиболее частых местных осложнений является образование жидкостных коллекторов; Атлантская классификация выделяет следующие их типы:
- жидкостное скопление, сопутствующее интерстициальному отечному панкреатиту
- острое перипанкреатическое скопление жидкости
- панкреатическая псевдокиста (формируется через 4 недели)
- жидкостное скопление, сопутствующее некротическому панкреатиту
- острое некротическое скопление
- отграниченный некроз (формируется через 4 недели)
Острое перипанкреатическое скопление жидкости
Может быть обнаружено в первые 4 недели от начала клинической картины. Выглядит как скопление гомогенного жидкостного содержимого без внутреннего солидного компонента. Оно ограниченно фасциальными пространствами брюшины и не имеет собственных стенок. Чаще всего локализуются в области малого сальника и переднем параренальном пространстве, однако могут «мигрировать» в области малого таза и средостения.
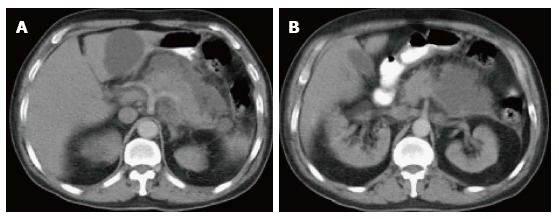
Рисунок 6 | На аксиальных КТ-сканах в портовенозную фазу поджелудочная железа слегка увеличена и несколько гетерогенно накапливает контрастное вещество.
Вентральнее железы можно увидеть скопление гомогенной жидкости без видимых стенок. Содержимое скопления не накапливает контраст. Эти признаки характерны для острого перипанкреатического скопления жидкости.
Около половины ОПСЖ формируется в первые 48 часов от начала процесса и разрешаются самостоятельно в течении месяца. При отсутствии осложнений и клинических проявлений не требуют хирургического вмешательства.
При КТ жидкостное содержимое низкой плотности (HU), на МР-томограммах — гиперинтенсивного сигнала в Т2 и гипоинтесивного (особенно заметно на фоне интенсивного сигнала от окружающей жировой клетчатки) — в Т1 и градиент-эхо.
Панкреатическая псевдокиста
О псевдокисте можно говорить через 4 недели от начала процесса — она представляет собой сохраняющееся скопление жидкости без солидного компонента, ограниченное четко определяемой стенкой.
При КТ стенки псевдокисты демонстрируют накопление контраста, больше выраженное в паренхиматозную фазу (что отражает присутствие грануляционной ткани). При МРТ же контрастное усиление можно заметить уже на ранних постконтрастных сканах, а своего пика оно достигает по прошествии около 5 минут после введения, что характерно для фиброзной ткани. Содержимое кисты не накапливает контраст.
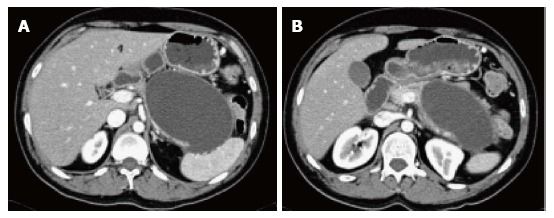
Рисунок 7 | Аксиальные КТ-сканы в позднюю портовенозную фазу контрастирования.
Определяется крупная овальной формы с четкими стенками псевдокиста, расположенная спереди тела и хвоста ПЖ, связанная с масс-эффектом на прилежащие отделы кишечника и ткань железы.
Иногда псевдокисты могут сообщаться с протоком поджелудочной железы, и обнаружение этой связи (при помощи МРХПГ) полезно для дальнейшего ведения пациентов.
Большинство псевдокист разрешаются спонтанно. Частым осложнением является инфицирование, которое может проявить себя наличием пузырьков газа. Однако отсутствие последних не исключает наличия осложнений; при клиническом подозрении стоит провести аспирационную биопсию содержимого.
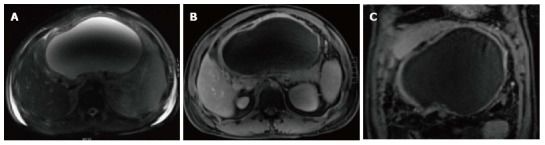
Рисунок 8
Аксиальные Т2 спин-эхо Т2ВИ (А), аксиальные и корональные постконтрастные 3D-GRE T1ВИ (В, С) демонстрируют наличие крупного жидкостного образования с четко определяемыми стенками (последние накапливают контрастное вещество) в области малого сальника. Содержимое гомогенное (гиперинтенсивная область в вентральных отделах обусловлена артефактом).
Диагноз: псевдокиста.
Острое некротическое скопление
Обнаруживается в первые 4 недели; важно помнить, что острое некротическое скопление может сопровождать только некротизирующий панкреатит. Некроз может вовлекать как паренхиму железы, так и перипанкреатическую клетчатку. Характерным КТ-признаком является наличие солидных компонентов в жидкостном скоплении; эти компоненты могут быть разных размеров и количества, а сами скопления могут быть как единичными, так и множественными.
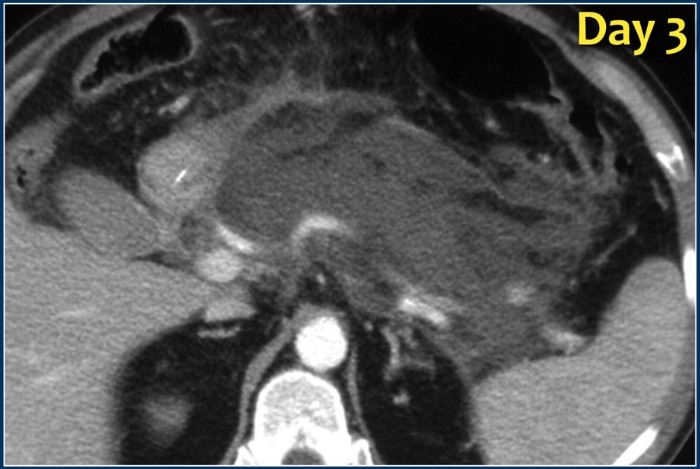
Рисунок 9
На аксиальном КТ-скане можно заметить скопление неоднородного жидкостного содержимого впереди от поджелудочной железы, большая часть паренхимы которой не накапливает контрастное вещество.
В первую неделю может быть сложно отличить некротическое скопление от перипанкреатического скопления жидкости — оба могут выглядеть как гомогенное жидкостное содержимое повышенной плотности; но по прошествии времени некротические включения становятся более заметными. МРТ и УЗИ также могут быть полезны для определения солидного содержимого.
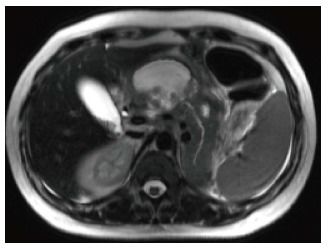
Рисунок 10 | Острое некротическое скопление.
Аксиальное турбо-спин-эхо Т2-взвешенное изображение. Впереди от поджелудочной железы определяется жидкостное скопление (гиперинтенсивного МР-сигнала), которое начинается от области шеи железы, которое сообщается с главным протоком железы. На фоне жидкостного содержимого можно увидеть включения низкого в Т2 сигнала — некротический детрит.
Отграниченный некроз
Формируется через 4 недели от начала процесса; является скоплением жидкости с солидными включениями, которое обязательно связано с некротизирующим панкреатитом и имеет сформированные стенки. Внутреннее солидное содержимое не накапливает контрастное вещество, стенки образования — накапливают так же, как и стенки псевдокисты.
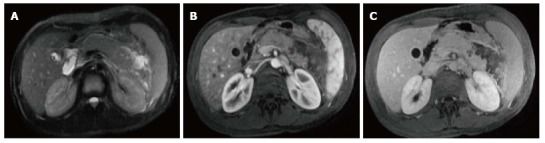
Рисунок 11 | Отграниченный некроз.
Аксиальные Т2 спин-эхо Т2ВИ (А), аксиальные и корональные постконтрастные 3D-GRE T1ВИ (В, С). В области перехода тела железы в хвост визуализируется область низкого в Т2 сигнала, которой на постконтрастных сканах соответствует зона нарушения перфузии. Также можно увидеть ограниченное стенкой скопление гетерогенного жидкостного содержимого.
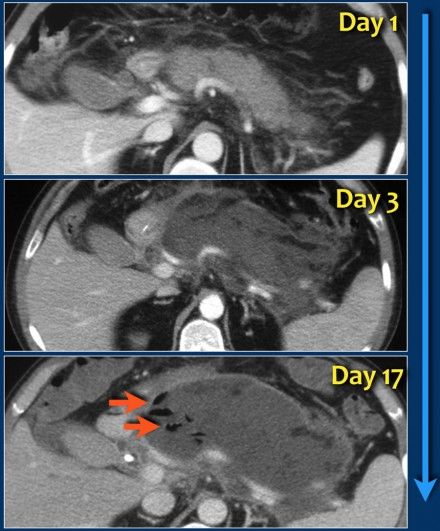
Рисунок 12 | Развитие инфицированного отграниченного некроза
На аксиальном постконтрастном КТ-скане, сделанном в первый день начала клинической картины железа выглядит диффузно увеличенной, окружающая жировая клетчатка тяжиста. При исследовании, проведенном на третий день вся ткань железы практически не накапливает контрастное вещество (некротизирующий панкреатит). На семнадцатый день можно увидеть сформированный, ограниченный стенкой коллектор с неоднородным содержимым, внутри которого визуализируются пузырьки газа (стрелка) — признак инфицированного некроза.
Тактика радиолога
Как уже было сказано, визуализация является необходимой для подтверждения диагноза ОП только если клинические и лабораторные данные сомнительны.
Однако лучевая картина в первые сутки от начала клинических проявлений может сбивать с толку: зачастую области некроза еще не успели сформироваться. Поэтому рентгенологу позволительно быть «ленивым» и не рекомендовать проведение КТ с контрастированием только что поступившему пациенту, а отложить процедуру (помните о лучевой нагрузке и возможных реакциях гиперчувствительности на контрастное вещество!). Наиболее четкая картина перфузионных нарушений формируется по прошествии недели от начала клинических проявлений
А вот в случаях, когда подозревается билиарный панкреатит, не стоит откладывать проведение МРХПГ, т.к. более ранняя экстракция конкремента улучшает прогноз для пациента.

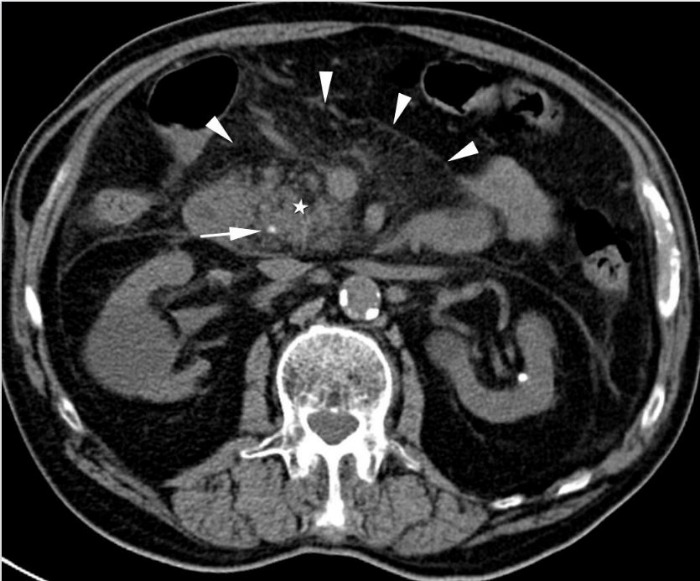
Рисунок 13 | Холедохолитиаз.
На нативном аксиальном КТ определяется плотный конкремент в общем желчном протоке на уровне головки ПЖ (звездочка). Тяжистость перипанкреатической жировой клетчатки говорит об интерстициальном панкреатите.
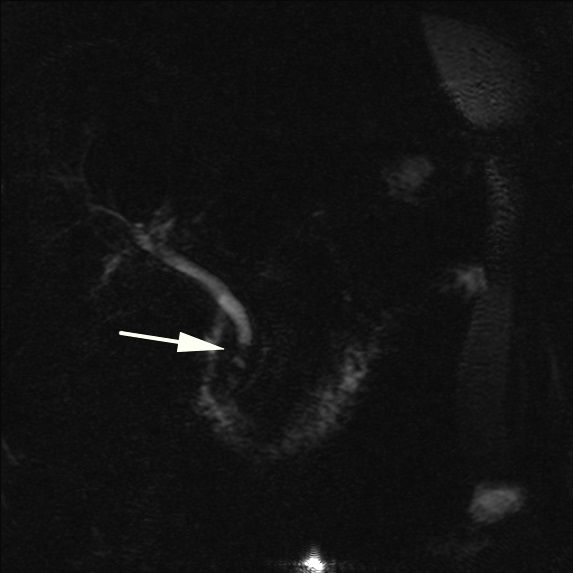
Рисунок 14
МРХПГ показала наличие конкремента в общем желчном протоке (стрелка, указывающая на дефект наполнения).
Источники
- Banks P. A. et al. Classification of acute pancreatitis—2012: revision of the Atlanta classification and definitions by international consensus //Gut. – 2013. – Т. 62. – №. 1. – С. 102-111.
- Федоровский В. В. СОВРЕМЕННАЯ МЕЖДУНАРОДНАЯ КЛАССИФИКАЦИЯ ОСТРОГО ПАНКРЕАТИТА-ОЧЕРЕДНОЙ ПЕРЕСМОТР //Journal of Siberian Medical Sciences. – 2015. – №. 3.
- Busireddy K. K. et al. Pancreatitis-imaging approach //World journal of gastrointestinal pathophysiology. – 2014. – Т. 5. – №. 3. – С. 252.
- O’Connor O. J., McWilliams S., Maher M. M. Imaging of acute pancreatitis //American Journal of Roentgenology. – 2011. – Т. 197. – №. 2. – С. W221-W225.
- Xiao B., Zhang X. M. Magnetic resonance imaging for acute pancreatitis //World journal of radiology. – 2010. – Т. 2. – №. 8. – С. 298.
- Олег Круглов. Радиография; Пересмотренная Атлантская классификация острого панкреатита – https://radiographia.info/article/peresmotrennaya-atlantskaya-klassifikaciya-ostrogo-pankreatita
- Thomas Bollen, Marieke Hazewinkel and Robin Smithuis. The radiology assistant; Pancreas – Acute Pancreatitis 2.0 – 2012 Revised Atlanta Classification of Acute Pancreatitis – https://www.radiologyassistant.nl/en/p550455dae5806/pancreas-acute-pancreatitis-20.html
- также по материалам ECR online 2018: W. Schima; Vienna. AT A-675 – A. Understanding the Atlanta 2012 classification of acute pancreatitis
Источник