Парез кишечника при остром панкреатите
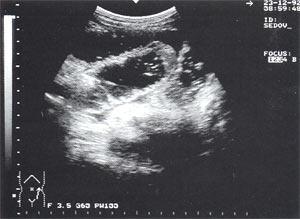
Парез кишечника – состояние, сопровождающее многие тяжелые заболевания и характеризующееся постепенным уменьшением тонуса кишечной стенки и параличом мускулатуры кишечника. Основные проявления пареза кишечника: равномерное вздутие живота, тошнота, рвота, отсутствие кишечных шумов, эксикоз, тахикардия, вторичная дыхательная недостаточность. Диагностика включает обзорную рентгенографию, УЗИ и КТ органов брюшной полости, колоноскопию, ирригоскопию. Лечение пареза кишечника комплексное: консервативная стимуляция моторики, симптоматическая терапия, декомпрессия кишечника, хирургические мероприятия.
Общие сведения
Парез кишечника является довольно распространенным проявлением патологии внутренних органов. Так, паралич мускулатуры кишечной стенки в 25% случаев развивается на фоне острой патологии органов брюшной полости, реже – при тяжелых заболеваниях сердечно-сосудистой системы, легких, при генерализованной инфекции, эндогенной интоксикации. Среди хирургических пациентов всех профилей парез кишечника диагностируется лишь у 0,2%. Более 70% больных с этой патологией находятся в возрасте старше 60 лет, поэтому кишечный паралич обычно считают заболеванием старческого возраста. Между тем, парез кишечника также может встречаться у новорожденных, детей разного возраста, беременных. Паралитическая непроходимость кишечника у беременных является очень тяжелой патологией, развивающейся в одном случае на 50 тыс. беременностей. Чаще всего данное состояние возникает во втором либо третьем триместре, характеризуется высоким уровнем опасности, как для матери, так и для ребенка.
Парез кишечника
Причины
Парез кишечника может развиться в результате интраперитонеального либо ретроперитонеального воспалительного процесса (при перитоните, забрюшинных флегмонах и других заболеваниях). Причиной данной патологии может быть нарушение кровоснабжения кишечника с развитием ишемии (при разрыве аневризмы брюшного отдела аорты, острой коронарной недостаточности и необратимой ишемии миокарда) или нарушение иннервации (при травматическом или опухолевом повреждении спинного мозга, угнетении синтеза ацетилхолина в нервных окончаниях, приеме блокаторов кальциевых каналов). Рефлекторный парез развивается при почечной колике, осложненном течении пневмонии. Также возможно нарушение моторики при эндогенных и экзогенных интоксикациях, оперативных вмешательствах.
В патогенезе пареза кишечника выделяют несколько стадий. На первом этапе формируется паралич гладкой мускулатуры кишечника, перистальтика постепенно замедляется, вплоть до полной остановки моторики кишечной стенки. Вторая фаза характеризуется застоем жидкого содержимого и газов в просвете тонкого и толстого кишечника, за счет чего прогрессивно растет внутрикишечное давление, а также диаметр кишки. Третий этап связан с нарастанием интоксикации, формированием полиорганной недостаточности. Парез кишечника может локализоваться как в определенном отделе кишечника, так и поражать всю тонкую и толстую кишку.
Риск развития пареза кишечника выше у пациентов, принимающих определенные медикаменты (способные угнетать перистальтику), имеющих серьезные дисэлектролитные и метаболические расстройства, особенно на фоне тяжелой инфекционной и интеркуррентной патологии.
Симптомы пареза кишечника
Пациенты с парезом кишечника предъявляют жалобы на вздутие живота; умеренные распространенные боли в животе, не имеющие четкой локализации и не склонные к иррадиации; тошноту и рвоту. В начале заболевания в рвотных массах содержится съеденная пища, желудочный сок; с течением времени рвотные массы приобретают каловый характер. Около 40% пациентов жалуются на запоры и отсутствие отхождения газов, однако у другой половины газы и кал могут отходить даже после развития клиники пареза кишечника. То же касается и повышения температуры – субфебрильная лихорадка отмечается не более чем у половины больных, чаще всего это говорит о наличии осложнений (перфорация кишечной стенки, перитонит).
Значительное вздутие живота на фоне пареза кишечника приводит к смещению диафрагмы и сдавлению органов грудной полости. Клинически это проявляется одышкой, поверхностным дыханием, тахикардией, артериальной гипотензией. Кроме того, длительная рвота на фоне пареза кишечника может приводить к обезвоживанию, проявляющемуся сухостью слизистых и кожи, снижением темпа диуреза.
При осмотре обращает на себя внимание прогрессирующее увеличение окружности живота (в некоторых случаях гастроэнтерологи и хирурги учитывают этот признак при оценке степени тяжести пареза кишечника). При пальпации живот умеренно болезненный (как при наличии ишемических процессов в стенке кишки, так и без них); аускультативно обращает на себя внимание значительное уменьшение интенсивности или полное отсутствие кишечных шумов. Определяется положительный симптом Лотейссена – на фоне полной тишины в брюшной полости выслушиваются дыхательные шумы, сердечные тоны. Пальцевое исследование прямой кишки выявляет расширенную и пустую ректальную ампулу.
К осложнениям пареза кишечника относят ишемию кишечной стенки с последующей перфорацией и перитонитом. Самопроизвольные перфорации случаются редко, но частота этого осложнения значительно возрастает при проведении колоноскопии и других вмешательств. Существует несколько признаков, указывающих на высокую вероятность прободения кишки: увеличение диаметра начальных отделов толстого кишечника (слепая кишка) более 120 мм, длительность пареза кишечника более шести суток. Летальность увеличивается в два раза при увеличении диаметра более 140мм, в пять раз – при длительности заболевания более семи суток.
Кровотечения встречаются довольно редко, в основном связаны с предшествующей патологией кишечника, тяжелой ишемией кишечной стенки. Если ишемия прогрессирует, формируется некроз, проявляющийся появлением пузырьков газа, как в толще кишечной стенки, так и в портальной вене. После регресса патологических изменений возможно формирование дивертикулов кишечника.
Диагностика пареза кишечника
Консультация гастроэнтеролога и хирурга позволяет установить клинические критерии пареза кишечника: наличие кишечной непроходимости, исключение механических причин этого состояния, установление этиологических факторов пареза.
Наименее чувствительным методом диагностики пареза кишечника считается обзорная рентгенография органов брюшной полости в трех позициях (вертикально, горизонтально, латеропозиция). На снимках визуализируются равномерно заполненные газом петли тонкой и толстой кишки, горизонтальные уровни жидкости (при этом типичные чаши Клойбера отсутствуют), расположенные на одном уровне. Основным критерием является отсутствие механических факторов непроходимости.
УЗИ и МСКТ органов брюшной полости являются более специфическими и чувствительными методиками, во время которых выявляются растянутые кишечные петли, горизонтальные уровни жидкости, повышенная пневматизация кишки. КТ позволяет точно определить наличие или отсутствие причин для пареза и непроходимости кишечника, выявить газ в толще его стенки, определить степень ишемии тонкой и толстой кишки.
Дифференцировать механическую и динамическую непроходимость (парез кишечника) позволяет ирригоскопия – в пользу пареза говорит полное заполнение толстого кишечника контрастом менее чем за четыре часа. Более безопасным и эффективным является выполнение колоноскопии с последующей декомпрессией кишечника. Дифференцировать парез кишечника следует с механической кишечной непроходимостью, копростазом, некоторыми инфекционными и паразитарными заболеваниями.
Лечение пареза кишечника
Лечение пациентов с парезом кишечника должно проводиться в отделении интенсивной терапии либо хирургии, с переводом в отделение гастроэнтерологии после улучшения состояния. Начинают терапию с консервативных мероприятий: разгрузки кишечника путем выведения газов (толстый желудочный зонд, газоотводная ректальная трубка), отмены энтеральной нагрузки, терапии основного заболевания (причины развития пареза кишечника), коррекции водно-электролитных и метаболических нарушений. В качестве мероприятий, улучшающих состояние пациента и ускоряющих разрешение пареза, рекомендуют использование жевательной резинки (существует ряд научных работ в области гастроэнтерологии, указывающих на стимуляцию перистальтики при жевании), умеренную физическую активность, коленно-локтевое положение больного.
Консервативная терапия включает медикаментозную стимуляцию перистальтики неостигмином. Первое введение препарата осуществляется под тщательным контролем гемодинамики, в случае развития брадикардии вводят атропин. Если после первого введения неостигмина перистальтика не усилится, рекомендуется начать его непрерывное инфузионное введение в течение как минимум суток – эффективность такой тактики не менее 75%. Введение неостигмина запрещено при констатации механической непроходимости кишечника, ишемических изменений или перфорации стенки кишки, а также при наличии беременности, тяжелых некорректируемых нарушений ритма, бронхоспазма и почечной недостаточности. Использование других препаратов для стимуляции перистальтики не рекомендовано, так как они обладают низкой эффективностью и повышенной частотой осложнений.
Существует три методики нехирургической декомпрессии кишечника: введение толстого зонда под рентгенологическим контролем, колоноскопия с последующим введением дренажа, чрескожная пункция слепой кишки и цекостомия. Показаниями к применению данных методик являются: увеличение диаметра толстого кишечника более 100 мм; длительность пареза кишечника более трех суток в сочетании с отсутствием эффекта от консервативной терапии на протяжении 48 часов; отсутствие положительной динамики от лечения неостигмином или наличие противопоказаний к его назначению. Методом выбора является колоноскопия, однако ее проведение запрещено при перитоните, перфорации кишки. Следует отметить, что изолированная колоноскопия эффективна у четверти пациентов, в то время как сочетание колоноскопии с введением дренажных трубок – практически в 90% случаев.
Чрескожную цекостомию назначают пациентам с высоким риском интраоперационных осложнений, при неэффективности консервативной терапии и колоноскопии с декомпрессией. Открытое оперативное вмешательство используется при отсутствии эффекта всех перечисленных выше мероприятий, при наличии перфорации кишки и перитонита. Проводится открытая цекостомия, резекция пораженного отдела кишечника. После хирургического лечения наркотические анальгетики не назначаются, так как они способны угнетать моторику кишечной трубки.
Прогноз и профилактика пареза кишечника
Прогноз при парезе кишечника значительно варьирует в зависимости от возраста пациента и наличия осложнений. Наибольшая летальность отмечается при наличии такого осложнения, как перфорация кишки – до 40%. У больных старше 65 лет возможно рецидивирование пареза кишечника (у каждого пятого) с формированием хронического илеуса. Специфической профилактики пареза кишечника не существует, вторичная профилактика заключается в своевременном выявлении и лечении патологии, которая может осложниться данным состоянием.
Источник

УЗИ сканер HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Введение
В России за последние годы отмечена тенденция к увеличению количества больных острым панкреатитом, частота которого достигает 2,5 – 8,4% среди пациентов с острыми хирургическими заболеваниями органов брюшной полости [1]. В странах Западной Европы, в частности, в Дании с 1979 по 1992 гг., частота острого панкреатита увеличилась с 26,8 до 35,4 на 100000 населения [15], т.е. на 25%. По данным М. В. Гринева [8], из всех больных с острым панкреатитом деструктивные формы отмечены у 16,2%, которые при прогрессировании приводят к летальности почти в 50% случаев [4].
Благодаря новым методам исследования (УЗИ, КТР, ЯМР) улучшилась ранняя диагностика острого панкреатита и его осложнений, появилась возможность динамического наблюдения за больными в процессе лечения. Для широкой практики особый интерес представляет ультразвуковая диагностика – неинвазивный, неионизирующий метод, который можно применять многократно, не причиняя вреда больному. С помощью эхографии стало возможным эффективно проводить не только диагностические, но и лечебные малоинвазивные вмешательства на поджелудочной железе – биопсию, дренирование патологических образований и т.д. [4, 6, 8].
Несмотря на интенсивное внедрение эхографии в практику и определенные успехи в изучении возможностей метода, в литературе еще недостаточно освещены вопросы, касающиеся деталей ультразвуковой семиотики острого панкреатита. Не конкретизирована эхографическая картина острого панкреатита в зависимости от стадии заболевания, мало отражены вопросы, касающиеся диагностики осложнений острого панкреатита, особенно редких, но клинически значимых [2, 5, 9 – 14, 16]. У пациентов, лечившихся оперативно по поводу острого панкреатита, актуальной остается проблема ультразвукового мониторинга в послеоперационном периоде. Практически не изучена роль данных ультразвукового исследования для выработки индивидуальной тактики лечения и прогнозирования возможных осложнений у каждого конкретного больного.
Материалы и методы
В основу работы положены данные 534 УЗ-исследований у 278 пациентов с острым панкреатитом, находившихся на лечении в городской клинической больнице N 9 за период 1992-1995 гг. Исследования проводились с помощью ультразвукового сканера, оснащенного конвексным датчиком 3,5 МГц и секторным – 5 МГц.
Результаты
На основе наших наблюдений выявлены следующие сонографические особенности острого панкреатита:
Изменения непосредственно в поджелудочной железе:
- увеличение размеров поджелудочной железы (рис. 1) – отмечено в 88% случаев. Нормальные размеры поджелудочной железы: головка 3-4,5 см; тело 2,5 – 3 см; хвост 3-4 см;
- нечеткость контуров – 90,6% случаев;
- увеличение расстояния между задней стенкой желудка и передней поверхностью поджелудочной железы свыше 3 мм и достигающее 10 – 20 мм, что характеризует отек парапанкреатических тканей, отмечено в 53% наблюдений (рис. 1);
- изменение эхогенности железы: повышение – 85,6% случаев (рис. 2); нормальная – 8,6% случаев; понижение – 5,8% случаев.
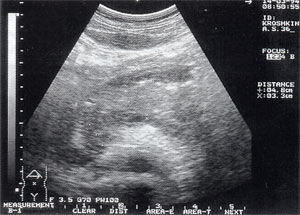
Рис. 1. Острый панкреатит, деструктивная форма. Увеличение размеров поджелудочной железы, нечеткость контуров, увеличение расстояния между задней стенкой желудка и поджелудочной железы.
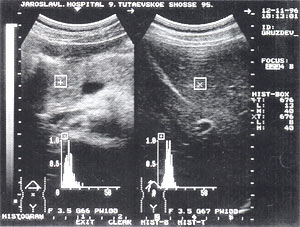
Рис. 2. Острый панкреатит, повышение эхогенности поджелудочной железы (по сравнению с эхогенностью печени).
Изменения в брюшной полости, являющиеся косвенными признаками острого панкреатита и относящиеся к его осложнениям:
Оментобурсит (рис. 3) встречается в 28,4% случаев (из них 48% у мужчин и 52% у женщин). Некоторые авторы обозначают эту патологию как “псевдокиста поджелудочной железы”. Отмечен объем таких образований от 5мл (малые объемы необходимо дифференцировать с сосудистыми аневризмами) до 3 л и более. Скорость формирования оментобурсита при остром панкреатите от 2 – 4 дн. от начала заболевания до 2 – 4 нед. При ультразвуковом исследовании оментобурсит представлен в виде анэхогенного образования с четкими контурами, неправильной или округлой формы, чаще с однородной структурой, с толщиной стенок 0,2 – 0,4 см. При эхографическом мониторинге утолщение стенки до 0,5 – 1,0 см с появлением неоднородности структуры следует расценивать как сонографический признак абсцедирования.
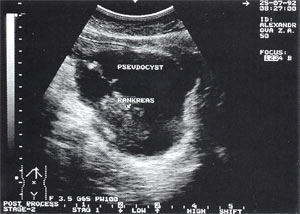
Рис. 3. Псевдокиста поджелудочной железы при остром панкреатите в виде анэхогенного образования с четкими контурами, однородной структурой, с наличием гиперэхогенных включений (детрит поджелудочной железы).
Свободная жидкость в брюшной полости – отмечена в 18% случаев (рис. 4), из них 80% у мужчин и 20% у женщин. Жидкость в объеме до 100 мл определяется только в одной анатомической области ( чаще в малом тазу), более 100 мл – по боковым каналам и в других отделах брюшной полости. В первые дни развития острого панкреатита жидкость гомогенная, после 6-12 сут. часто структура неоднородная из-за “нитевидных” включений (как правило, фибрин).

Рис. 4. Расширенные петли тонкого кишечника до 3,5 см, заполненные жидким содержимым на фоне свободной жидкости в брюшной полости.
Билиарная гипертензия – встречается в 13% случаев, из них 25% у мужчин и 75% у женщин. При эхографии отмечается расширение внутрипеченочных желчных протоков, общего печеночного протока и общего желчного протока. При отсутствии холедохолитиаза билиарная гипертензия как правило наблюдается при очаговом панкреонекрозе в области головки поджелудочной железы.
Инфильтраты брюшной полости – обнаруживаются в 5,4% случаев (рис. 5, 6), в том числе 64% у мужчин и 36% у женщин. Как правило, инфильтрируется большой сальник (оментит), визуализирующийся в виде образования повышенной эхогенности с нечеткими неровными контурами, неоднородной структурой, с участками пониженной эхогенности, которые могут свидетельствовать о формировании в нем абсцессов. Размеры инфильтратов от 5 до 15 – 20 см.
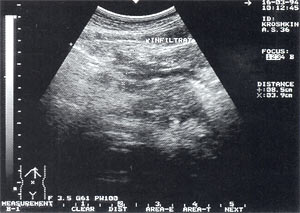
Рис. 5. Инфильтрат в брюшной полости в проекции большого сальника – представлен образованием неправильной формы с нечеткими контурами, неоднородной структурой, с наличием гипер- и гипоэхогенных участков. Размер инфильтрата 8,5 х 3,9 х 5,3см.
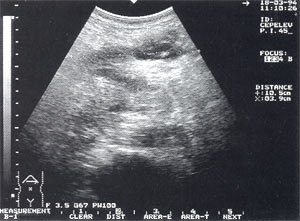
Рис. 6. Инфильтрат в проекции большого сальника с анэхогенным включением до 4 см (абсцедирование).
Забрюшинные флегмоны – встречаются в 4,3% случаев (рис. 7), из них 67% у мужчин и 33% у женщин. В 95% случаев диагностирована левосторонняя локализация флегмоны, которая определялась в виде анэхогенного или гипоэхогенного образования чаще щелевидной или овальной формы. Как правило, причиной развития данного осложнения является распространение панкреатического секрета по забрюшинному пространству из псевдокисты, иногда доходящее до паховой области. Панкреатогенный паранефрит можно рассматривать как вариант забрюшинной флегмоны.
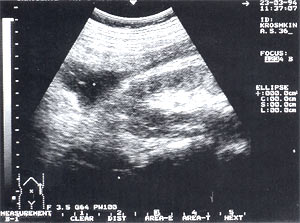
Рис. 7. Забрюшинная флегмона слева – анэхогенное образование неправильной формы с нечеткими контурами. Сканирование проведено из левой поясничной области.
Гидроторакс – встречается в 2,2% случаев, одинаково часто у мужчин и женщин, с преимущественно левосторонней локализацией.
Тромбоз в системе воротной вены – отмечается в 1,5% случаев (рис. 8 а, б) и достаточно хорошо может быть определен, по нашему мнению, без допплеровского исследования. При признаках портальной гипертензии обязательно должно выполняться прицельное ультразвуковое исследование сосудов системы воротной вены. Тромбы могут быть одиночными и множественными. Они локализуются как в самой воротной вене, так и в селезеночной и верхнебрыжеечной венах.
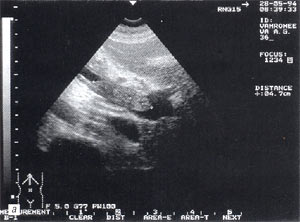
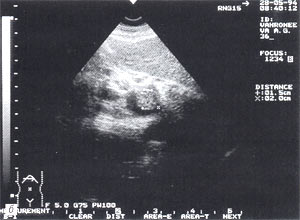
Рис. 8. Тромбоз воротной вены. Просвет вены полностью обтурирован изоэхогенным образованием с четкими контурами, неоднородной структурой, длиной до 4,7 см (а – cагиттальный срез, б – поперечный срез).
Парез кишечника – встречается в 1,4% случаев (см. рис. 4), из них 75% у мужчин и 25% у женщин. Характеризуется расширением петель тонкого кишечника до 3 – 5 см с заполнением их жидким содержимым и регистрируемой “маятникообразной” перистальтикой.
Гидроперикард – встречается в 0,4% случаев.
Восходящий медиастенит, отмечаемый другими авторами, нами не наблюдался.
Абсцессы поджелудочной железы – встречаются как правило на фоне уже имеющихся ультразвуковых признаков хронического панкреатита.
Разрывы псевдокист поджелудочной железы при ультразвуковой диагностике наблюдались у 2 больных (0,7%).
Кровоизлияние в псевдокисту поджелудочной железы с формированием организованной гематомы (рис. 9) отмечено у 1 пациента (0,35%).
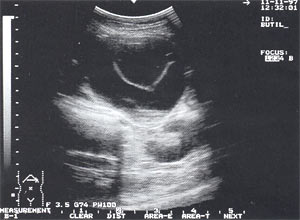
Рис. 9. Псевдокиста поджелудочной железы в виде анэхогенного образования с четкими контурами, в котором определяется другое анэхогенное образование с капсулой 0,2 – 0,3 см (на операции – псевдокиста с организовавшейся гематомой).
Псевдокисты поджелудочной железы с атипичной локализацией (в печени, селезенке, перидуоденально и т.д.) выявлены у 2 больных – 0,7% (рис. 10).
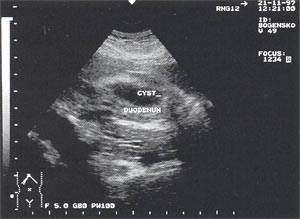
Рис. 10. Атипично расположенная псевдокиста поджелудочной железы (парадуоденально) в виде анэхогенного образования округлой формы с четкими контурами, однородной структурой, размером до 4,5 см, расположенного рядом с двенадцатиперстной кишкой.
Инфаркты селезенки (1 больная – 0,35%) – на фоне тромбоза воротной вены с портальной гипертензией.
Разрывы селезенки вследствие портальной гипертензии (нами не наблюдались).
Панкреатогенные паранефриты – обнаружены у 2 пациентов, что составило 0,7% (рис. 11).
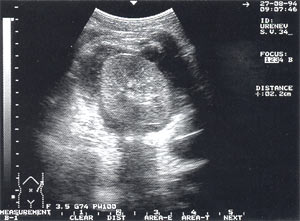
Рис. 11. Левосторонний панкреатогенный паранефрит, визуализирующийся в виде жидкостного образования, окружающего почку со всех сторон. Поперечный срез.
Заключение
Проведенное исследование показывает, что ультразвуковая диагностика должна быть обязательным элементом диагностического алгоритма у больных острым панкреатитом. Для повышения диагностической ценности эхографии необходима определенная последовательность в выполнении ультразвукового исследования: детальный осмотр парапанкреатических тканей и самой железы; осмотр всех отделов брюшной полости на предмет свободной жидкости и инфильтратов; осмотр плевральных полостей и полости перикарда на наличие выпота; детальный осмотр внутри- и внепеченочных желчных протоков; прицельный осмотр сосудов системы воротной вены; исследование забрюшинного пространства; динамическое наблюдение (частота повторного УЗИ определяется степенью тяжести заболевания и вероятностью развития осложнений).
Для улучшения получаемых результатов УЗИ могут быть рекомендованы следующие технические приемы:
- при плохой визуализации хвост поджелудочной железы лучше исследовать через селезенку или левую почку;
- для улучшения визуализации поджелудочной железы можно применять заполнение желудка 500 – 800 мл дегазированной жидкости (воды);
- использовать датчики с различной частотой излучения для более детального исследования патологических очагов, расположенных на разном расстоянии от датчика;
- использовать полипозиционное сканирование с дозированной компрессией на брюшную стенку для улучшения визуализации исследуемых органов, что позволяет “раздвигать” петли кишечника, создавая тем самым дополнительное “акустическое окно”;
- применять ультразвуковую фистулографию с жидкими и газообразующими растворами (фурацилин, новокаин, “Echovist”) для определения полостей при наличии панкреатических свищей [7], что может быть предметом отдельных исследований.
Литература
- Скуя Н. А. Заболевания поджелудочной железы. – М.: Медицина, 1986.
- Зубарев А. Р., Григорян Р. А. Ультразвуковое ангиосканирование. – М.: Медицина, 1990.
- Филин В. И., Костюченко А. А.. Неотложная панкреатология. – СПб., 1994.
- Нестеренко Ю. А., Михайлусов С. В., Иманалиев М. Р. Ультразвук в диагностике и лечении панкреонекроза/ Сб. научн. тр. Пленума проблемной комиссии по неотложной хирургии. – М.: 1994. – С. 26 – 29.
- Баранов Г. А., Могутов М. С, Завьялова Н. И. Ультразвуковая диагностика тромбоза воротной вены как редкого осложнения острого панкреатита/ Сб. науч. тр. международной конференции “Новые технологии в диагностике и в хирургии органов билиопанкреатодуоденальной зоны”. – М.: 1995. – С. 4 – 5.
- Белокуров ГО. Я., Уткин А. К., Жохов В. К., Белокуров С. Ю., Могутов М. С. Предпосылки использования прецизионной техники в лечении ложных кист поджелудочной железы/ Сб. научн. тр. международной конференции “Новые технологии в диагностике и в хирургии органов билиопанкреатодуоденальной зоны”. М.: 1995. – С. 78.
- Буйлов В. М., Могутов М. С, Карпов Н. Р. Ультразвуковая фистулография с “Echovist-300” в хирургии и урологии. – Материалы II съезда Ассоциации специалистов ультразвуковой диагностики в медицине. – М.: 1995. – С. 80.
- Гринев М. В., Красногоров В. Б., Рысс А. С, Веселов В. С, Смелянский А. И., Алексеенко Е. Н. Эффективная тактика лечения деструктивного панкреатита на основе раннего плазмафереза и малоинвазивных хирургических вмешательств/ Сб. научн. тр. “Малоинвазивные вмешательства в хирургии”. М.: 1996. – С. 257.
- McCormick P. A., Chronos N., Burroughs A. К., Mclntyre N., McLaughlinJ.E. Pancreatic pseudocyst causing portal vein thrombosis and pancreatico – pleural fistula.In: Gut (1990 May) 31(5):561-3.
- Fernandez-Cruz-L., Margarona-E., Llovera-J., Lopez-Boado-M. A., Saenz-HT. Pancreatic ascites. Hepatogastroenterology. 1993 Apr; 40(2): 150-4.
- Nishida-K., Terai-Y., Nojiri-L, Kato-M., Higashijima-M., Takagi-K., Adashi-R. A case of pancreatic pseudocyst with intracystic hemorrhage and repeated gastrointestinal bleeding. Nippon-Ronen-Igakkai-Zasshi. 1993 Aug; 30(8): 714-9.
- Sonak-R., Stock-W., Janzik-U., Hayduk-K., Borchard-F. Duodenal duplication cyst – a rare cause of acute recurrent pancreatitis. Leber-Magen-Darm. 1993 Sep; 23(5): 211-5.
- De-Ronde-T., Van-Beers-B., de-Canniere-L., Trigaux-JP., Melange-M. Thrombosis of splenic artery pseudoaneurysm complicating pancreatitis. Gut. 1993 Sep; 34(9): 1271-3.
- Hamm-B., Franzen-N. Atypically located pancreatic pseudocysts in the liver, spleen, stomach wall and mediastinum: their CT diagnosis. Rofo-Fortschr-Geb-Rontgenstr-Neuen-Bildgeb-Verfahr. 1993 Dec; 159(6): 522-7.
- Worning-H. Acute pancreatitis in Denmark. Ugeskr-Laeger. 1994 Apr 4; 156(14): 2086-9.
- Yasuda I., Tomita E., Nishigaki Y., Ino Y., Shimizu H., Yamada T., Kawamura H., Kuroda T., Takahashi T., Nagura K. A case of portal vein thrombosis subsequent to acute pancreatitis. Nippon Shokakibyo Gakkai Zasshi (1995 Apr) 92(4):820-5.

УЗИ сканер HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Источник
