Послеоперационный панкреатит после резекции желудка
Порой, человек не совсем понимает одного из смыслов счастья – счастье быть здоровым. Не бережет заложенное природой здоровье, пренебрежительно относится к нему, его сигналам.
А когда осознает катастрофичность ситуации, бывает, уже совсем мало времени на принятие решения, и жизнь уже рисуется в мрачных красках. Иногда выходом является только операция: плановая или срочная. В этой статье разберем удаление поджелудочной железы последствия и жизнь после.

Как выгляди и какие функции у поджелудочной железы?
Поджелудочная железа — орган, который встроен в пищеварительную цепочку человеческого организма, выполняет в ней определенный важные функции. Железа имеет вытянутую форму, состоит из трех частей (головка, тело и хвост), располагается сзади желудка, соединена протоками с двенадцатиперстной кишкой.
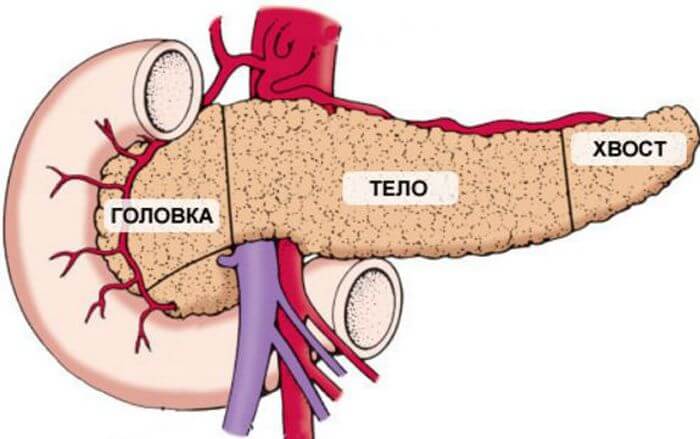
Через эти протоки в кишку поступает панкреатический сок, необходимый для переваривания пищи, расщепления ее составляющих (белки, жиры, углеводы) и дальнейшего усвоения организмом. Еще поджелудочная нужна для синтеза гормонов, участвующих в работе разных систем организма.
Все слышали медицинский термин «инсулин», необходимы для поддержания уровня сахара в крови. Так вот, поджелудочная железа является кузницей этого гормона. И не только его (глюкагон, соматостатин, панкреатический полипептид).
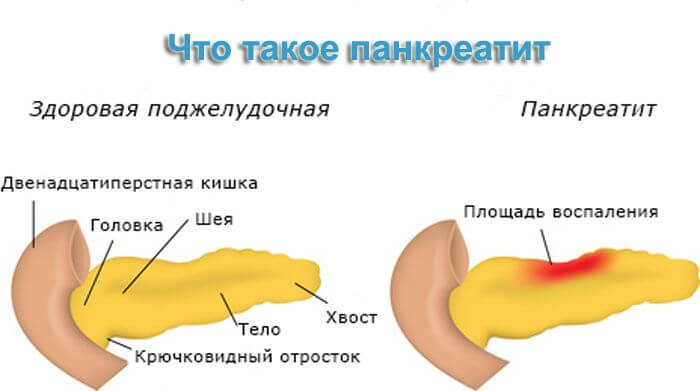
Нарушения в работе этого органа провоцирует такую серьезную болезнь, как сахарный диабет, а также несут людям проблемы с перевариванием пищи. Воспаление поджелудочной железы ведет к ряду заболеваний, которые лечатся медикаментозно, например, панкреатит.
Хирургическое вмешательство
Однако не всегда удается с помощью лекарственной терапии восстановить все функции органа. Врач может рекомендовать операцию на поджелудочной железе, причем, иногда экстренно, для спасения жизни пациента. Услышав такой «приговор» больной задается вопросом: можно ли жить без поджелудочной железы? Каковы последствия? Эти вопросы будоражат его сознание, не дают успокоиться, адекватно взглянуть на ситуацию. Как жить? – роятся в голове мысли и не дают покоя.
Операция по удалению поджелудочной железы (панкреэктомия) назначается обычно при раке. Если не удается сохранить весь орган человека, вследствие, его полного поражения, врач настаивает – удалить поджелудочную железу! Могут быть вырезаны и близлежащие органы (Селезенка, верхняя часть желудка, желчный пузырь).
Делается операция под общим наркозом. Перед ее проведением больной сдает анализы, в том числе на онкомаркеры, ферменты, проходит УЗИ, КТ, с помощью лапароскопа врач оценивает степень поражения органов, может быть назначен также курс химиотерапии. Во многих случаях врачи-хирурги удаляют лишь больные части железы. Это в медицинской терминологии получило название — резекция поджелудочной железы.
Показания к частичному удалению органа следующие:
- Частичное отмирание тканей (например, при панкреонекрозе).
- Травмы.
- Опухоли.
- Кровотечения
- Кисты, свищи.
- Обострился хронический панкреатит (терапия не помогает).
Операция на поджелудочной железе чаще проводятся по удалению ее головки или хвоста. Считается сложным видом, т. к. железа «спрятана» глубоко в брюшине и доступ к ней затруднен, плюс близость других органов (возможное их заражение), несут тоже свои сложности в работе хирурга.
Риски
Есть, конечно, определенные риски и опасности для пациента, такие так: открывающиеся кровотечения, занесение инфекций в организм, возможные проблемы с анестезией, случайно поврежденные соседние органы.В зависимости от тяжести состояния поступившего больного на операционный стол, его возраста, степени ожирения, состояния сердечно-сосудистой системы и других факторов, будет зависеть, как быстро пациент начнет восстанавливаться.
Реабилитация
Процесс реабилитации долгий, сопровождающийся ноющими болями, тяжело, порой, заживающей раной на месте шва. Больной переводится на строгую диету. Но постепенно идет на поправку. Человек, перенесший операцию, конечно, не может полностью восстановить полноценное здоровье.
Последствия операции на поджелудочной железе непременно проявятся. Теряется вес, нарушается пищеварение, назначаются больному пожизненно инъекции инсулина, препараты ферментной терапии, т. к. организм не вырабатывает уже ни инсулин, ни ферменты, приобретается диабет.
Жизнь без железы
Может ли человек ощущать себя в относительной гармонии с миром после столь серьезной операции?
Без поджелудочной железы прожить можно, и даже очень долго. Люди живут, работают, создают семьи, рожают детей. Главное, научиться новым правилам и приемам, мочь принять ситуацию такой уже, как есть.
Это раньше считалось, что жизнь без поджелудочной железы не жизнь, а мучения, ведущие к смерти. А сегодня, как таковой критичной, ситуации нет. Медицина шагнула далеко вперед, колоссальные наработки, опыт накоплен в международной практике и нашей медицине.
Поможет в восстановлении и специальная диета после удаления поджелудочной железы. Сначала очень строгая (сразу после операции: голодовка, одно питье). В первую неделю можно человеку употреблять кашки на воде (гречневую, рисовую), омлет из белков яиц, супы из перетертых овощей, очень капуста полезна, хлеб сухой, нежирный творог.
Пища не должна быть жирная, как можно меньше углеводов, сбалансированные белки, постепенно вводится мясо нежирное и рыба. Питание дробное, исключает сахар и уменьшает в разы соль.
Без железы как без одного из органов пищеварения возможно жить. Пациент потихоньку с помощью родных будет приходить в норму, свыкаясь с некими новыми для себя обстоятельствами, требованиями, понимая необходимость в отказе от пагубных привычек. Что делать? Жизнь одна и жизнь дороже!
Источник
Операции при раке поджелудочной железы могут выполняться с целью радикального удаления опухоли, либо паллиативно, для уменьшения объема опухолевой ткани и/или устранения жизнеугрожающих осложнений.
В большинстве случаев злокачественные опухоли поджелудочной железы диагностируются на поздних стадиях, поэтому радикальная операция возможна приблизительно у 15% пациентов. Стоит отметить, что такие операции – длительные, объемные, травматичные и сопряжены с высоким риском осложнений как в интраоперационном, так и послеоперационном периодах. Вместе с тем это единственный метод радикального лечения, который позволяет продлить жизнь пациента на несколько лет.
При выборе тактики лечения врачи опираются на критерии операбельности рака поджелудочной железы, разработанные NCCN, с помощью которых определяются резектабельные, нерезектабельные и пограничные опухоли.
Состояние резектабельности опухоли поджелудочной железы:
- опухоль не затрагивает верхнюю брыжеечную артерию;
- чревный ствол и печеночная артерия интактны;
- верхняя брыжеечная вена и воротная вена проходимы.
Состояние пограничной операбельности опухоли:
- верхняя брыжеечная вена инфильтрирована опухолью менее, чем на половину своей окружности, либо имеется контакт опухолевых очагов со стенкой сосуда;
- инфильтрирован футляр печеночной артерии на небольшом протяжении. В этом случае оперирующий врач должен быть готов к резекции сосуда с последующим проведением пластики;
- возможно вовлечение в опухолевый процесс короткого сегмента верхней брыжеечной вены или воротной вены, при этом стенка сосуда выше и ниже места инфильтрации должна быть абсолютно неизмененной.
Признаки нерезектабельности опухоли:
- окружность верхней брыжеечной артерии инфильтрирована более чем наполовину;
- опухолевая инфильтрация чревного ствола, при которой нет возможностей выполнения реконструктивной пластики после удаления пораженного сегмента сосуда;
- полная окклюзия верхней брыжеечной вены и/или воротной вены.
Следует учитывать, что погранично-операбельные опухоли — это весьма условный термин. Раньше считалось, что вовлечение в процесс сосудистых образований является препятствием для оперативного лечения. Современные возможности хирургии позволяют удалить опухоль и восстановить целостность сосудистых коллекторов с использованием аллогенных трансплантатов. Возможность проведения таких операций зависит от навыков оперирующего хирурга и технической оснащенности клиники, поэтому пациентов с признаками пограничной резектабельности рекомендуется направлять в лечебные учреждения более высокого уровня для получения второго экспертного мнения и повторной оценки резектабельности.
Боль при злокачественных опухолях ПЖ
Боль при раке поджелудочной железы носит сильный, мучительный характер и локализуется в верхней части живота. Она может отдавать в позвоночник, грудину, сердце, лопатки и руки. В ряде случаев именно боль является первым признаком заболевания, в других ситуациях она присоединяется позже — при прогрессировании злокачественного процесса.
При установленном диагнозе для облегчения симптома пациент должен принимать анальгетики, в том числе наркотического ряда. Как правило, используется морфин. Предпочтение отдается препаратам для перорального применения. Но при развитии обструкции пищеварительного тракта или нарушении акта глотания возможно применение пластыря или инъекций.
Для пациентов, которые не переносят анальгетики или при снижении их эффективности можно применять блокаду солнечного сплетения (сеть нервных окончаний, располагающихся позади поджелудочной железы). Анальгезирующие препараты вводятся либо чрескожно под контролем КТ, либо под контролем эндоскопического УЗИ через стенку желудка. Эффект достигается у 50-90% больных и держится от 1 месяца до года.
Виды оперативного вмешательства при злокачественных опухолях поджелудочной железы
К радикальным операциям при раке поджелудочной железы относят:
- Гастропанкреатодуоденальная резекция — частичное удаление желудка, поджелудочной железы и двенадцатиперстной кишки с сохранением пилоруса или без него. Такие вмешательства применяются при локализации опухоли в головке ПЖ.
- Панкреатэктомия — полное удаление поджелудочной железы. Такие вмешательства используются при локализации опухоли в теле и хвосте железы. Для хирурга технически полное удаление железы несколько проще, чем частичное, но после таких вмешательств пациент должен будет пожизненно принимать гормональнозаместительную и ферментозаместительную терапию.
- Дистальная панкреатэктомия — производится резекция тела и хвоста поджелудочной железы, а также удаление селезенки. Такие операции выполняются крайне редко ввиду особенностей распространения опухолевого процесса.
Радикальные операции могут выполняться как открытым лапаротомическим доступом, так и с помощью эндоскопического оборудования через несколько маленьких проколов. Но и в том и другом случае необходимо удаление лимфатических узлов в стандартном объеме.
Следует отметить, что решение о возможности проведения радикального вмешательства может приниматься непосредственно во время операции, после ревизии тканей, куда чаще всего распространяется опухоль. Не исключены случаи, когда при обнаружении признаков нерезектабельности врач прекращает первоначально запланированную операцию и приступает к паллиативным вмешательствам.
К паллиативным операциям относят:
- операции внутреннего желчеотведения — эндоскопическое стентирование желчных протоков, наложение билиодигестивных анастомозов и др.;
- операции, направленные на организацию наружного дренирования желчных путей — чрезкожное чреспеченочное дренирование.
Такие операции не избавляют пациента от опухоли, но устраняют или предотвращают развитие таких жизнеугрожающих состояний, как механическая желтуха или непроходимость органов ЖКТ. Дело в том, что опухоли поджелудочной железы могут врастать или сдавливать желчные протоки, приводя к застою желчи и, как следствие, к критическому повышению уровня билирубина. Если вовремя не купировать такое состояние, оно может привести к гибели пациента. После паллиативных операций продолжительность жизни пациентов в среднем составляет около 8 месяцев.
Радикальные операции при опухолях головки поджелудочной железы
При раке, локализующемся в головке поджелудочной железы, проводят гастропанкреатодуоденальную резекцию. Во время операции удаляют 2/3 желудка, желчный пузырь, головку ПЖ, двенадцатиперстную кишку и лимфатические узлы. Только таким образом можно резецировать все поврежденные раком ткани и пути его метастазирования.
В ряде случаев желудок не трогают. Этот вариант хирургического вмешательства называется операцией по Лонгмире/Траверсо. При ней также возможно сохранение пилоруса — сфинктера привратника желудка. Такая техника позволяет предотвратить развитие ряда проблем с пищеварением. Заключительным этапом выполняют восстановление непрерывности пищеварительного тракта и выведение протоков пищеварительных желез в желудок или кишечник с помощью анастомозов.
Возможными проблемами после таких вмешательств могут быть:
- несостоятельность анастомозов из-за их разрушения едким соком поджелудочной железы;
- нехватка пищеварительных ферментов;
- резекция желудка может привести к миграции кишечных бактерий в вышележащие отделы ЖКТ и развитию инфекционных осложнений;
- развитие демпинг-синдрома — поступление в тонкий кишечник необработанной пищи. При этом возникают приступы учащенного сердцебиения, скачок артериального давления, диарея, снижение массы тела вплоть до кахексии. В тяжелых случаях приступы тахикардии могут длиться несколько часов.
Тотальная панкреатэктомия
Полное удаление поджелудочной железы производится при злокачественном поражении всех тканей органа в случаях, когда опухоль не выходит за его пределы. Во время операции удаляется вся железа, селезенка, часть желудка, желчный пузырь, и часть тонкой кишки.
После операции пациента ожидают глубокие нарушения в области углеводного обмена и пищеварения. Чтобы скорректировать эти состояния необходимо пожизненно принимать инсулин и пищеварительные ферменты.
Последствия операций на поджелудочной железе
Еще несколько десятков лет назад хирурги предпочитали не связываться с поджелудочной железой вообще, поскольку ее повреждение во время операции могло стать фатальным для больного. Сегодня, с развитием хирургических технологий и фармацевтики возможна жизнь даже после тотальной панкреатэктомии.
В целом последствия после онкологических операций на поджелудочной железе наблюдаются всегда, так как происходит полная или частичная утрата органа, ответственного как за углеводный обмен, так и за секрецию пищеварительных ферментов. Чем больший объем железистой ткани удален, тем сильнее будут выражены нарушения. Чтобы компенсировать эти последствия, необходимо придерживаться ряда правил:
- строгая диета;
- соблюдение режима питания;
- прием ферментозамещающих препаратов;
- коррекция углеводного обмена с помощью инъекций инсулина.
Диета и режим питания
Первые несколько дней после операции пероральное питание невозможно, поэтому пациент должен получать поддерживающие растворы внутривенно. Затем все же следует отдавать предпочтение кормлению через рот.
Пищу следует принимать маленькими порциями 5-6 раз в день. Она должна быть приготовлена на пару или протушена. В целом рекомендуется отдавать предпочтение блюдам, богатым белками и, по возможности, отказаться от «легких» углеводов и жиров.
Необходимо исключить ряд продуктов, например, свежий хлеб и выпечку, все виды приправ, острых блюд, копчености, маринады, шоколад, сладости, молочные продукты. Более подробные рекомендации даст лечащий врач с учетом особенностей конкретного клинического случая.
Во время каждого приема пищи необходимо принимать ферментные добавки. Это могут быть альфа-амилаза, фестал, креон, микразим и др. Они нормализуют переваривание пищи и устраняют чувство тяжести, тошноту и явления диспепсии.
Терапия инсулином
При полном удалении поджелудочной железы для нормализации углеводного обмена необходима терапия синтетическим инсулином, аналогично тому, как это делают больные с сахарным диабетом. Подбор дозы и режим введения препарата определяется врачом-эндокринологом индивидуально для каждого пациента.
Восстановление
Операции при злокачественных опухолях поджелудочной железы обширны и травматичны, поэтому пациент будет нуждаться в уходе. В первые 2-3 дня он будет находиться в условиях реанимации. Если все в порядке, пациента переводят в профильное отделение.
Для того чтобы избежать таких осложнений как тромбозы, спайки и пневмонии, рекомендуется ранняя мобилизация, если нет противопоказаний. В первое время пациенту достаточно просто переворачиваться в постели и выполнять специальные упражнения и дыхательную гимнастику. Чтобы снизить нагрузку на область швов, их можно придерживать подушкой. После того как больной окрепнет, ему разрешается сидеть и вставать с постели для коротких прогулок. На этом этапе уже можно использовать послеоперационный бандаж. В среднем, сроки госпитализации варьируют в пределах 2-4 недель, в зависимости от способа проведения операции (лапароскопически и лапаротомически).
После резекции поджелудочной железы все пациенты теряют вес. Чтобы пищеварительная система приспособилась к новым условиям работы, необходимо 1,5–3 месяца. Весь этот период нужно строго следовать рекомендациям касательно диеты. При полном удалении железы этих ограничений придется придерживаться пожизненно, также, как и принимать гормонозаместительные и ферментные препараты.
Прогноз
Радикальная операция при злокачественной опухоли поджелудочной железы – это единственный способ полностью устранить рак. Если возникают рецидивы, принимается решение о выборе дальнейшей тактики лечения. Это может быть химиотерапия, радиотерапия, гормональное лечение и другие методы.
У врачей Европейской клиники имеется большой опыт лечения пациентов, страдающих раком поджелудочной железы. Несмотря на достаточно агрессивную форму заболевания, пациентам с диагнозом «рак поджелудочной железы» помочь можно всегда. В одних случаях удается достичь увеличения продолжительности жизни, в других — снятия болевого синдрома и улучшения качества жизни.
Источник
Библиографическое описание:
Ибадильдин, А. С. Современные принципы диагностики и лечения послеоперационного панкреатита / А. С. Ибадильдин, Ж. А. Джакашева, Олжас Нурланулы Апырбаев. — Текст : непосредственный // Молодой ученый. — 2015. — № 11 (91). — С. 655-658. — URL: https://moluch.ru/archive/91/19574/ (дата обращения: 31.12.2020).
Актуальность: быстрый темп развития компьютерных технологий в медицине и новейших методов обследования пациентов позволяет нам в кратчайшие сроки установить диагноз послеоперационных осложнений. Одним из таких осложнений является послеоперационный панкреатит.
В большинстве случаев послеоперационный панкреатит развивается в первые 3–4 суток после операции. Частота данного осложнения после лапаротомий составляет 0,7–25,6 %, а при операциях на поджелудочной железе возрастает до 32,7–50 % (Б. И. Альперович 1991 г., Р. В. Вашетко с соавт.) [1].
Клиника послеоперационного панкреатита вариабельна, каких-либо патогномоничных симптомов не имеет. Этим объясняется постоянный поиск новых, информативных методов распознавания его [2].
Выявление гомеостазиологических нарушений, их коррекция, своевременная релапаротомия предопределяют исход заболевания больных послеоперационным панкреатитом и являются актуальными проблемами [3].
Летальность при послеоперационном панкреатите остается высокой — 24,5 %, а при деструктивных формах достигает 50–60 % и не имеет тенденции к снижению (Р. В. Вашетко).
Цель исследования: оптимизировать алгоритм диагностики, лечения послеоперационного панкреатита и определить оптимальные сроки релапаротомии для снижения летальности.
Задачи:
– изучить частоту развития панкреатита после операции на органах брюшной полости,
– выявить частоту клинико-лабораторных проявлений послеоперационного панкреатита,
– определить значимость неинвазивных и малоинвазивных методов диагностики послеоперационного панкреатита,
– определить необходимость и оптимальные сроки релапаротомии,
– разработать эффективные способы санации брюшной полости.
Материалы и методы. Мы проанализировали результаты лечения 6689 больных оперированных в военном госпитале г. Алматы с 1982 по 2012 гг. по поводу заболеваний и травм органов брюшной полости.
Операции были проведены на следующих органах: поджелудочной железе — 253(10 случаев послеоперационного панкреатита — 4 %), желудке и двенадцатиперстной кишке — 1268 (24 случая — 1,9 %), билиарном дереве — 3152 (28 случаев — 0,9 %), печени — 1231 (3 случая — 0,2 %), селезенке и прочих органах — 785 (6 случаев — 0,8 %) (см. Диаграмма 1).
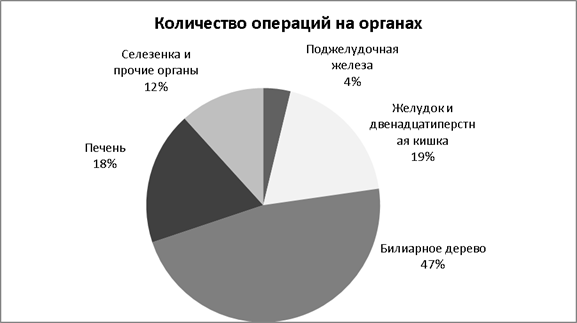
Рис. 1.
Послеоперационный панкреатит развился у 71 больного (1,1 %). Мужчин — 59 (83 %), женщин — 12 (17 %). Возраст больных колеблется в пределах от 25 до 74 лет.
Клинически, лабораторно и УЗИ-подтвержденный послеоперационный панкреатит возник на 3–4 сутки, только у 8 человек на 7–8 сутки. Клиническая картина его характеризовалась скудностью и непостоянством симптоматики.
Частыми клиническими проявлениями были: боль в верхних отделах живота — 68 (95,8 %); тахикардия — 64 (90 %); парез кишечника, не поддающийся лечению — 52 (73,2 %); рвота — 47 (66,2 %); гипертермия — 38 (53,5 %); напряженный мышечный дефанс в эпигастрии — 33 (46,5 %); иктеричность кожи — 28 (39,4 %); положительный симптом Щеткина-Блюмберга — 25 (35,2 %); коллапс — 12 (16,9 %); психоз — 12 (16,9 %); икота — 10 (14 %) (см. Диаграмма 2).
В общем анализе крови отмечался выраженный лейкоцитоз в 62 (81,3 %) случаях, сдвиг лейкоцитарной формулы влево в 30 (42,3 %) случаях, токсическая зернистость лейкоцитов в 22 (31 %) случаях. Биохимический анализ крови показал гипербилирубинемию за счет прямой фракции у 25 (35 %) пациентов, повышение уровня АЛТ и АСТ у 21 (30 %), гипергликемию у 15 (21 %) и повышение амилазы у 32 (45 %) пациентов. Диастазурия имелась в 35 (49 %) случаях, но только у 23 (32 %) больных достигла значительных цифр.
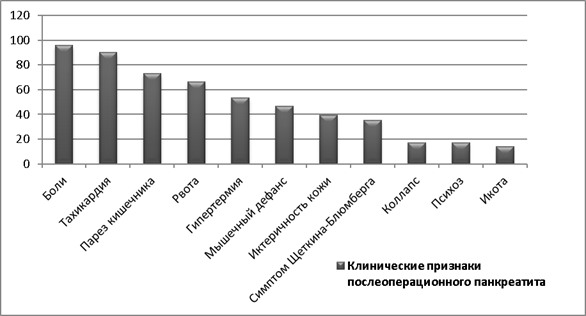
Рис. 2.
Вышеперечисленный симптомокомплекс показывает глубину гомеостатических нарушений и не является патогномоничным для данного осложнения. Для облегчения постановки диагноза, мы выделили основные симптомы, такие как: боли в верхних отделах живота, выраженный парез кишечника, тахикардия, гипертермия. Значительную роль в диагностике сыграла диастазурия и использование специальных методов исследования. При рентгенологическом обследовании у 32 (45 %) больных выявлены косвенные признаки панкреатита: вздутие поперечно-ободочной кишки, левосторонний реактивный плеврит, симптом «дежурной кишки», симптом «вырезанной кишки», симптом «отсеченной ободочной кишки». Ультразвуковое исследование позволяет выявить увеличение размеров, размытость контуров поджелудочной железы, наличие выпота в сальниковой сумке. После операции на органах верхнего отдела брюшной полости не всегда удается визуализировать поджелудочную железу: из 68 обследованных больных ценная информация получена у 41. Наиболее информативными являются компьютерная томография и диагностическая видеолапароскопия.
В клинике мы начинаем лечение с функционального покоя поджелудочной железы: декомпрессии желудка, локальной гипотермии, парентерального, а в последние годы и энтерального питание. Проводим коррекцию нарушений гемостаза, детоксикацию, улучшение реологии крови, купирование проявлений синдрома системного воспалительного ответа. Широко используем управляемую гемодилюцию с форсированным диурезом [4].
Особое значение мы придаем мероприятиям по блокированию повреждающего воздействия ферментативного токсического экссудата, играющего важную роль на ранних стадиях тяжелого послеоперационного панкреатита и применению различных методик выведения токсических компонентов из тканевых депо.
При проведении курса интенсивной консервативной терапии у 49 (69 %) из 71 больных отмечалось субъективное и объективное улучшение состояния через 36–48 часов от начала лечения: купировались признаки интоксикации, нормализовались показатели крови и диастазы.
В 22 (31 %) случаях консервативное лечение не имело эффекта. Прогрессивное ухудшение состояния пациентов, нарастание симптомов ферментной токсемии, появление признаков перитонита явились показанием к релапаротомии. 16 пациентов взяты на операцию с диагнозом послеоперационный панкреатит. У 6 больных был выставлен диагноз: высокая тонкокишечная непроходимость (4), недостаточность швов анастомоза (2).
Релапаротомии произведены в следующие сроки с момента появления симптомов осложнения: через 6–24 часов — у 9 больных, на 2–4 сутки — у 12, на 5 сутки — у 1 (см. Диаграмма 3). При релапаротомии диагностированы жировой панкреонекроз у 14, геморрагический панкреонекроз у 8 больных. Перитонит диагностирован в 19 случаях (86,4 %).
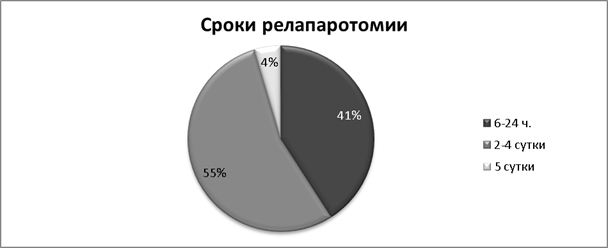
Рис. 3.
Во время операции по поводу тяжелого послеоперационного панкреатита хирург должен решить несколько проблем. Наиболее сложной и ответственной является выбор рациональной хирургической тактики.
У 12 больных после релапаротомии проводилась программированная видеолапароскопическая санация брюшной полости по нашей методике с использованием специального лапаропорта (патент № 19772 от 28.05.2008г.). Лапаропорт устанавливали и фиксировали на передней брюшной стенке. Через него выполнялась ревизия и санация брюшной полости эндохирургической стойкой фирмы «Карл Шторц». После окончания лечения лапаропорт удаляли, а фиксирующие его нити завязывали, закрывая дефект передней брюшной стенки [5].
Больные получали внутриаортальную инфузию лекарственных средств, антибиотикотерапию, управляемую гемодилюцию с форсированным диурезом. На фоне послеоперационного тяжелого течения с явлениями интоксикации, пареза кишечника у 10 (45,4 %) больных развились осложнения: у 5 (22,7 %) пневмония, у 3 (13,6 %) плеврит, у 2 (9,1 %) флегмона брюшной стенки. Двое (9,1 %) повторно 2 раза оперированы по поводу спаечной кишечной непроходимости и абсцессов брюшной полости. Проводилась иммунокоррегирующая и иммунозаместительная терапия. При анемии переливали свежецитратную кровь. Применяли анаболические гормоны и пиримидиновые производные, антистафилококковую плазму, антистафилококковый гамма-глобулин.
Умерло 6 больных, что составило 8,4 % от всех случаев послеоперационного панкреатита и 27,2 % после релапаротомий. У 5 на вскрытии геморрагический панкреонекроз, у 1 — жировой с распространением некротического процесса на забрюшинную клетчатку. Причиной летального исхода явилось у 5 больных прогрессирование панкреонекроза, у 1 профузное кровотечение из магистральных артериальных сосудов.
Выводы:
1. Доминирующими клиническими проявлениями послеоперационного панкреатита явились болевой синдром, выраженный парез кишечника, тахикардия, гипертермия;
2. Для ранней диагностики и коррекции лечения информативными оказались неинвазивные методы мониторирования — рентгенологическое, ультразвуковое исследования, компьютерная томография, клинико-лабораторные данные;
3. Неэффективность консервативной терапии в течении суток должна явиться показанием для релапаротомии;
4. Операция должна быть минимальной по объему;
5. Применение лапароскопического мониторирования позволило своевременно санировать и купировать прогрессирование послеоперационного панкреатита.
Литература:
1. Басенов Л. Н. Неотложная хирургия груди и живота. Руководство для врачей. СПб, Гиппократ, 2002 г.
2. Макаренко Г. П. Ведение больных общехирургического профиля в послеоперационном периоде, 1989 г.
3. Клиническая хирургия: Национальное руководство, 3 т. (редакция Савельев В. С., Карпенко А. И., Гальперин Э. И., Милонов О. Б.) — Медиа, 2002г., том — 2.
4. Неотложная хирургия органов брюшной полости (клиническое руководство) под редакцией Кондратенко П. Г., Русина В. И. Донецк, 2013 г.
5. Ибадильдин А. С.. Хирургические болезни. Алматы, 2010.
Основные термины (генерируются автоматически): послеоперационный панкреатит, брюшная полость, больной, поджелудочная железа, верхний отдел живота, компьютерная томография, парез кишечника, передняя брюшная стенка, тяжелый послеоперационный панкреатит, форсированный диурез.
Источник
