Современный классификация острый панкреатита
В.Е. ВОЛКОВ, Л. И. ЧЕРКЕСОВ,
С.В. ВОЛКОВ, Н.Н. ЧЕСНОКОВА
ОСТРЫЙ ПАНКРЕАТИТ: СОВРЕМЕННАЯ КЛАССИФИКАЦИЯ
И ОБЩИЕ ПРИНЦИПЫ ЛЕЧЕНИЯ
Чувашский государственный университет имени И.Н. Ульянова, Чебоксары
Представлен ретроспективный анализ лечения 461 больного острым панкреатитом за 2009-2013 гг. Отечная (интерстициальная) форма острого панкреатита установлена у 378 (82%) пациентов, некротическая форма – у 83 (18%) пациентов. Дана оценка клинических исследований по идентификации локальных жидкостных скополений с учетом международной классификации острого панкреатита (2012). Общая летальность больных острым панкреатитом составила 6, 1%, при некротической форме панкреатита – 32, 1%.
Ключевые слова: острый панкреатит, классификация, диагностика, локальные перипанкреатические жидкостные скопления, лечение.
Острый панкреатит ‒ одно из наиболее распространенных заболеваний органов брюшной полости, объединяемых термином «острый живот». В последние десятилетия отмечается рост заболеваемости острым панкреатитом, как в Российской Федерации, так и в странах Европы и США. Этот факт, вероятно, связан с улучшением ранней диагностики данного заболевания за счет усовершенствования лабораторно-инструментальных методов исследования [1, 2, 4].
Актуальность проблемы диагностики и лечения острого панкреатита обусловлена достаточно высокой летальностью, которая при некротической форме составляет 35-40% [2, 3]. Развитие различных осложнений, утяжеляет течение и ухудшает прогноз. У 20-30% пациентов острый панкреатит, неуклонно прогрессируя, приводит к развитию некроза ткани поджелудочной железы. При этом в 40-70% случаев уже через 3 недели с момента заболевания происходит инфицирование очагов некроза, что является ведущей причиной смерти больных острым панкреатитом. Необходимо отметить, что острым панкреатитом в большинстве случаев заболевают лица трудоспособного возраста. Высокие экономические затраты на лечение госпитализированных больных свидетельствуют о практической значимости данной проблемы.
Цель: уточнить практическую значимость новой международной классификации острого панкреатита и представить критерии ранней диагностики локальных перипанкреатических жидкостных скоплений.
Материалы и методы исследования. Проведен ретроспективный анализ лечения 461 больного острым панкреатитом, находящихся на стационарном лечении в хирургическом отделении БУ «Больница скорой медицинской помощи» Минздрава Чувашии за 2009-2013 гг. Из 461 больного отечная форма острого панкреатита отмечена у 378 (82%) пациентов, некротическая форма – у 83 (18%) пациентов.
Результаты и их обсуждение. Острый панкреатит ‒ системное полиэтиологическое заболевание, которое возникает в результате воздействия активированных ферментов на ткань поджелудочной железы с развитием отека или ограниченного, или обширного некроза. Основными этиологическими факторами заболевания являются злоупотребление алкоголем и его суррогатами, а также желчекаменная болезнь. При этом в последние годы острый панкреатит, развивающийся вследствие употребления алкоголя, наблюдается в среднем в 50-70% случаев, тогда как панкреатит билиарного происхождения ‒ в 40% случаев. Другими причинами заболевания являются открытые и закрытые травмы поджелудочной железы, в том числе связанные с операциями, а также с инструментальными исследованиями. Сравнительно редко этиологическими факторами являются эндокринные заболевания, прием некоторых лекарственных средств и т.д.
Основными звеньями патогенеза острого панкреатита являются обструкция панкреатического протока с развитием внутрипротоковой гипертензии, а также активизация ферментов поджелудочной железы на фоне усиленной панкреатической секреции. Блокада большого дуоденального сосочка желчными конкрементами является фактором механической обструкции, что препятствует нормальному оттоку секрета поджелудочной железы. Употребление алкоголя приводит к спазму сфинктера Одди, отеку слизистой оболочки и усилению внешнесекреторной функции железы за счет повышенной секреции соляной кислоты. Внутрипротоковая гипертензия приводит к повреждению клеточных и субклеточных мембран, гиперсекреции и активации протеолитических ферментов, в первую очередь, трипсина, с выходом их в интерстициальное пространство и развитием аутолиза ткани поджелудочной железы. Указанные патогенетические факторы приводят, в конечном итоге, к отеку и некрозу поджелудочной железы. Необходимо отметить, что при развитии острого панкреатита протеолитические ферменты, биологически активные полипептиды, продукты тканевого распада обладают вазоактивным действием и при попадании в системный кровоток оказывают генерализованное воздействие на органы и ткани, приводя к развитию критического состояния вследствие полиорганной недостаточности.
- На основании морфологических признаков повреждения поджелудочной железы и клинических особенностей течения заболевания Рабочей Группой специалистов по изучению острого панкреатита в 2012 г. была предложена новая международная классификация острого панкреатита [5], которая включает следующие формы:
- Отечная форма (интерстициальный панкреатит).
- Асептический панкреонекроз.
- Инфицированный панкреонекроз.
- Фазы развития панкреонекроза:
- Доинфекционная;
- Инфекционная.
- Стадии панкреонекроза:
- Ранняя;
- Поздняя.
- Степень тяжести острого панкреатита:
- Легкая степень;
- Средняя степень;
- Тяжелая степень.
- Виды локальных осложнений острого панкреатита:
- Острое перипанкреатическое жидкостное скопление;
- Панкреатическая псевдокиста;
- Острое некротическое скопление;
- Отграниченный некроз.
Интерстициальный панкреатит характеризуются воспалительным отеком ткани поджелудочной железы вследствие попадания в интерстиций небольшого количества активных ферментов, тогда как при панкреонекрозе возникают очаги деструкции ткани с развитием множественных кровоизлияний. Инфицирование зон некроза приводит к развитию инфицированного панкреонекроза и возникновению инфекционных осложнений.
Острый панкреатит легкой степени тяжести характеризуется отсутствием органной недостаточности, локальных и системных осложнений.
Острый панкреатит средней тяжести характеризуется наличием транзиторной (преходящей) органной недостаточности с длительностью течения менее 48 ч или возникновением локальных и системных осложнений.
Тяжелая форма острого панкреатита характеризуется наличием персистирующей органной недостаточности с длительностью течения более 48 ч.
Локальные осложнения острого панкреатита могут возникать как в доинфекционную, так и в инфекционную фазу развития заболевания и, как правило, утяжеляют его течение.
Острое перипанкреатическое жидкостное скопление в большинстве случаев наблюдается в первые четыре недели от начала развития острого панкреатита и обычно состоит из того или иного количества экссудата без наличия некротических масс, образующегося вследствие воспалительного отека паренхимы поджелудочной железы, выхода панкреатического сока через сеть концевых панкреатических протоков. Чаще всего данный тип скопления остается стерильным и рассасывается самостоятельно на фоне проводимого лечения. Согласно нашим исследованиям, чаще всего жидкостное скопление образуется в полости сальниковой сумки, забрюшинной клетчатке, в области левого поддиафрагмального пространства, нередко сочетаясь с образованием левостороннего плеврита.
Длительность существования острого перипанкреатического жидкостного скопления (более четырех недель) и отграничение его от окружающих тканей грануляционной или фиброзной тканью завершается образованием другого локального осложнения острого панкреатита ‒ псевдокисты.
Острое некротическое скопление чаще всего возникает на фоне деструктивного процесса в поджелудочной железе. В отличие от указанных выше жидкостных образований данный тип скопления характеризуется наличием жидкости и некротического детрита. При отграничении острого некротического скопления от окружающих тканей появляется возможность формирования отграниченного некроза.
Оценивая в целом новую международную классификацию острого панкреатита (2012), следует отметить отсутствие в ней нередко встречающихся локальных гнойно-септических осложнений этого заболевания, многие из которых таят опасность развития таких опасных осложнений, как распространенный гнойный перитонит, гнойный плеврит, сепсис и септический шок, острая полиорганная недостаточность. С учетом этих данных мы различаем следующие локальные гнойно-септические осложнения острого некротического панкреатита:<> – Панкреатический гнойный инфильтрат;
– Абсцесс сальниковой сумки;
– Гнойно-некротическая секвестрация поджелудочной железы и забрюшинной клетчатки;
– Инфицированная псевдокиста;
– Острое перипанкреатическое скопление жидкости;
– Сочетанные гнойно-септические осложнения.
Необходимо отметить, что более чем в 50% случаев отмечается сочетание локальных и распространенных гнойно-септических осложнений, утяжеляющих течение отсрого некротического панкреатита.
- Раннее распознавание острого панкреатита является залогом его эффективного лечения и благоприятного исхода. Согласно Международным рекомендациям 2012 г., диагностическими критериями острого панкреатита является триада признаков:
- Интенсивная абдоминальная боль опоясывающего характера с локализацией преимущественно в эпигастральной области;
- Увеличение уровня амилазы или липазы в 2-3 раза по сравнению с нормой;
- Характерные признаки поражения поджелудочной железы по данным УЗИ, КТ, МРТ.
Основными лабораторными признаками, свидетельствующими о вторичном инфицировании зон панкреатического некроза, являются нейтрофильный лейкоцитоз со сдвигом лейкоформулы влево, увеличение концентрации С-реактивного белка, прокальцитонина. На современном этапе целесообразно определение концентрации провоспалительных цитокинов ‒ ИЛ-1, ИЛ-6, TNF-альфа, трипсиноген-активированного белка, эластазы полиморфно-ядерных нейтрофилов, повышенный уровень которых свидетельствует о тяжелом течении острого панкреатита.
Наиболее информативными инструментальными методами диагностики острого панкреатита являются УЗИ, КТ, МРТ органов брюшной полости. УЗИ остается одним из наиболее доступных и информативных методов исследования. Эта безопасная неинвазивная методика позволяет выявить этиологический фактор острого панкреонекроза (конкременты желчевыводящих путей), отек и участки некроза поджелудочной железы, позволяет дифференцировать жидкостные образования. Но «золотым стандартом» диагностики на современном этапе является компьютерная томография органов брюшной полости. Данная методика позволяет четко визуализировать увеличение поджелудочной железы, очаги некроза, а также наличие осложнений, с высокой достоверностью разграничивать жидкостное скопление от плотных некротических масс. Наличие пузырьков газа в зоне деструкции, определяемое при КТ-исследовании, свидетельствует об инфицировании данного очага.
В настоящее время применяется дифференцированный подход к выбору лечебной тактики при остром панкреатите: от различных вариантов консервативного лечения в ранние сроки заболевания до разнообразных хирургических вмешательств при распространенных инфицированных формах панкреонекроза [1, 4].
Основными принципами консервативного лечения больных с острым панкреатитом являются:
‒ снижение панкреатической секреции, что достигается проведением тотального парентерального питания в течение первых 2-4 суток, декомпрессия желудка в течение 1-2 суток с помощью назогастрального зонда, назначение блокаторов Н2-рецепторов гистамина или ингибиторов протонной помпы, 5-фторурацила, соматостатина;
‒ инфузионная и дезинтоксикационная терапия с помощью введения коллоидных и кристаллоидных растворов внутривенно: от 3 до 5 литров и более в течение 3-7 дней;
‒ улучшение реологических свойств крови введением гепарина, реополиглюкина и т.д.;
‒ антибиотикотерапия с использованием препаратов широкого спектра действия (препараты выбора ‒ карбапенемы, цефалоспорины III-IV поколений или фторхинолоны II-III поколений в сочетании с метронидазолом). Показаниями к хирургическому лечению панкреонекроза являются наличие инфекционных осложнений, а также стойкая или прогрессирующая полиорганная недостаточность, сохраняющиеся симптомы системной воспалительной реакции независимо от факта инфицирования при проведении базисной консервативной терапии.
Использование консервативного и оперативного метода лечения позволило получить общую летальность у анализируемой группы больных панкреатитом в среднем 6, 1%, а при осложненных некротических формах ‒ 32, 1%.
- Литература
- Багненко С.Ф. Острый панкреатит современное состояние проблемы и нерешенные вопросы / С.Ф. Багненко, В.Р. Гольцов // Альманах института хирургии им. А.В. Вишневского, 2008. Т. 3 ‒ № 3 . ‒ С. 104-112.
- Волков В.Е. Острый некротический панкреатит / В.Е. Волков, С.В. Волков // Изд-во Чуваш. ун-та. 2009. ‒ 240 с.
- Волков В.Е. Ранняя диагностика и лечение локальных гнойно-септических осложнений у больных острым некротическим панкреатитом: учебное пособие / В.Е. Волков, Н.Н. Чеснокова, С.В. Волков // Чебоксары: Изд-во Чуваш. ун-та, 2015. – 60 с.
- Савельев В.С. Панкреонекрозы / В.С. Савельев, М.И. Филимонов, С.З. Бурневич // М.: Мед. Информ. Агенство, 2008. – 264 с.
- Banks P.A. Classification of acute pancreatitis – 2012 : Revision of the Atlanta classification and definitions by international consensus / P. Banks, T.L. Bollen, C. Dervenis et al. // Gut. – 2013. ‒ № 62 (1), P. 102-111.
СВЕДЕНИЯ ОБ АВТОРАХ:
Волков Владимир Егорович
заведующий кафедрой хирургических болезней ФГБОУ ВО «Чувашский государственный университет им. И.Н. Ульянова», доктор медицинских наук, профессор
Черкесов Леонид Ильич
профессор кафедры хирургических болезней ФГБОУ ВО «Чувашский государственный университет им. И.Н. Ульянова», кандидат медицинских наук
Волков Сергей Владимирович
профессор кафедры хирургических болезней ФГБОУ ВО «Чувашский государственный университет им. И.Н. Ульянова», доктор медицинских наук
Чеснокова Наталия Николаевна
аспирант кафедры хирургических болезней ФГБОУ ВО «Чувашский государственный университет им. И.Н. Ульянова»
Источник

Атлантская классификация острого панкреатита (ОП) — это международная мультидисциплинарная классификация тяжести острого панкреатита. Она является результатом работы международной группы экспертов и была представлена в 1992 году на международном симпозиуме в Атланте, США, а в 2012 году была пересмотрена. Эта классификация опирается на патоморфологические особенности разных типов острого панкреатита с учетом длительности его течения.
Согласно Атлантской классификации, чтобы поставить диагноз ОП, требуется наличие двух из следующих трех признаков:
- характерная абдоминальная боль (постоянная сильная эпигастральная боль, часто с иррадиацией в спину, с острым началом);
- показатели сывороточной липазы (амилазы) по крайней мере в 3 раза выше верхней границы нормы;
- характерные признаки ОП при КТ с контрастным усилением либо, реже, магнитно-резонансной томографии (МРТ) или трансабдоминальном УЗИ.
То есть, если диагноз острого панкреатита установлен на основании клинической картины и повышения уровня активности ферментов, необязательно немедленно проводить лучевую диагностику для его подтверждения.
АК выделяет следующие морфологические типы ОП:
- интерстициальный отечный панкреатит
- некротизирующий панкреатит, который, в свою очередь, подразделяют на:
- панкреатический паренхиматозный некроз
- перипанкреатический некроз
- панкреатический паренхиматозный некроз в сочетании с перипанкреатическим некрозом (наиболее часто встречаемый)
Все типы некротизирующего панкреатита могут быть стерильными или инфицированными; главным признаком, указывающим на инфицированность при доступных методах визуализации является образование пузырьков газа.
Для определения тяжести процесса нужно учесть наличие местных и общих осложнений.
Местные осложнения:
- острое перипанкреатическое скопление жидкости;
- панкреатическая псевдокиста;
- острое некротическое скопление и отграниченный некроз; а также
- нарушение эвакуации из желудка, тромбоз селезеночной и воротной вен и некроз ободочной кишки;
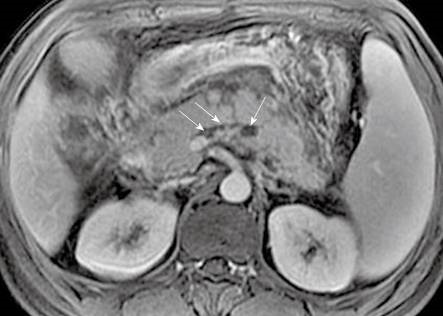
Рисунок 1 | Острый панкреатит, осложнившийся тромбозом селезеночной вены у мужчины 30 лет.
На аксиальной постконтрастной Т1ВИ можно увидеть дефекты наполнения в вовлеченных в процесс участках селезеночной вены (стрелки).
Определение как морфологического типа, так и местных осложнений во многом опирается на данные лучевых методов — и о них мы поговорим подробнее ниже.
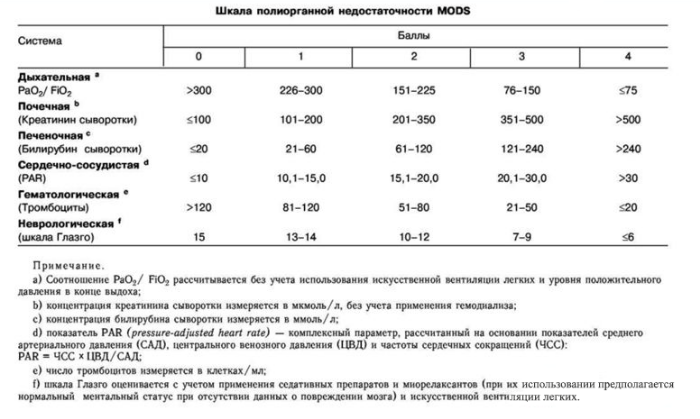
Общими осложнениями называют явления полиорганной недостаточности, которые могут быть переходящими (т. е. разрешаться в течение 48 часов) либо хроническими. Обострение уже существовавших сопутствующих заболеваний, таких как ишемическая болезнь сердца (ИБС), хронические заболевания легких, развившиеся вследствие ОП, также определяется как системное осложнение. Для определения органной недостаточности должны быть оценены три системы органов: дыхательная, сердечно-сосудистая и почечная. С этой целью используется модифицированная шкала Marshall (Табл. 1). Если имеется 2 и более баллов по данной шкале — присутствует органная недостаточность.
Таблица 1 | Шкала Marshall
По степени тяжести острый панкреатит (ОП) делится на легкий, средней тяжести и тяжелый.
- легкий ОП — нет признаков органной недостаточности, локальных или системных осложнений.
- средней тяжести ОП — признаки органной недостаточности, которая разрешается в течение 48 часов (преходящая органная недостаточность) и/или локальных или системных осложнений без продолжающейся органной недостаточности.
- тяжелый ОП — продолжающаяся более 48 часов органная недостаточность. Развитие инфицированного некроза у пациентов с продолжающейся органной недостаточностью связано с крайне высокой смертностью.
Поговорим о том, что представляют собой разные морфологические типы острого панкреатита и как они выглядят при лучевом исследовании.
Сразу оговоримся, что методом выбора в данном случае является КТ с контрастированием; УЗИ — зачастую менее информативный метод. МРТ выполняется реже из-за дороговизны и меньшей доступности метода, но может быть назначена в случае наличия противопоказаний к КТ (детский возраст, беременность, аллергические реакции на ионные контрастные вещества).
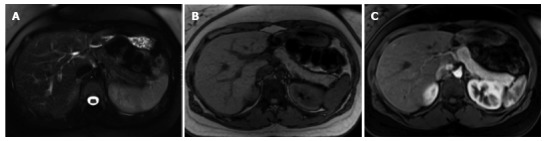
Рисунок 2 | Нормальная картина поджелудочной железы.
Т2ВИ с подавлением сигнала от жира (А) и GRE out-of-phase Т1ВИ (В) и постконтрастные Т1ВИ (С) в портовенозную фазу контрастирования.
Интерстициальный отечный панкреатит
Является воспалением паренхимы ПЖ и перипанкреатических тканей, но без видимых признаков тканевого некроза.
При КТ проявляется диффузным (редко — локальным) увеличением ПЖ в размерах, с гомогенным среднеинтенсивным накоплением контрастного вещества. Перипанкреатическая жировая клетчатка может выглядеть слегка «замутненной» или демонстрировать легкую тяжистость.
УЗИ-признаками являются увеличение размеров и гипоэхогенность ткани железы.
На МР-томограммах в Т1 взвешенных изображениях хорошо заметны увеличение размеров железы и размытость ее внешних границ; Т2-взвешенные томограммы (особенно с подавлением сигнала от жира) очень чувствительны и демонстрируют усиление сигнала от отечной ткани. Накопление контраста также гомогенное, может быть слегка пониженным в сравнении с картиной неизмененной поджелудочной железы.
Магнитно-резонансная холангиопанкреатография (МРХПГ) является крайне ценным методом для диагностики билиарного панкреатита: желчные конкременты четко визуализируются в виде участков «выпадения» сигнала.
Некротизирующий панкреатит
Процесс некроза, который может вовлекать либо ткань ПЖ и перипанкретические ткани, либо только перипанкертическую ткань, либо, реже всего, только паренхиму ПЖ.
Основной симптом некроза при КТ и МРТ с внутривенным контрастированием — область нарушения перфузии, т. е. зона, не накапливающая контрастное вещество; в первые недели эта область может выглядеть гетерогенно накапливающей контрастный препарат, а по прошествии времени (как правило, около недели) от начала симптомов формируются отграниченные области, которые явно не демонстрируют контрастного усиления.
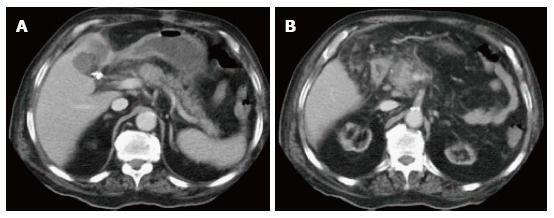
Рисунок 3
На аксиальных КТ-сканах в портовенозную фазу на уровне головки поджелудочной железы определяется участок нарушения перфузии, который не распространяется за пределы железы.
Лучше всего оценивать эти изменения на артериальной фазе контрастирования (наиболее ярко разница заметна в поздней артериальной и портовенозной фазах, когда неизмененная ткань ПЖ накапливает контрастный агент особенно интенсивно. Поздняя артериальная фаза (при КТ) наступает через 30–35 секунд после инъекционного или 15–20 секунд после болюсного введения контрастного препарата; должно определяться интенсивное контрастное усиление артерий и паренхимы органа; может также определяться незначительное количество контраста в портальной вене (из-за чего эта фаза также называется ранней портовенозной).
Обнаруженную по прошествии недели от начала симптомов область ткани ПЖ без контрастного усиления следует считать некрозом.
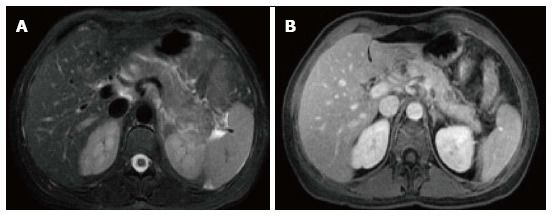
Рисунок 4 | Аксиальные спин-эхо Т2ВИ с подавлением сигнала от жира (А) и GRE Т1ВИ в портовенозную фазу контрастирования (В).
В проксимальной части хвоста железы определяется участок низкого Т2 сигнала, который демонстрирует снижение накопления контрастного препарата. Также можно увидеть тяжистость окружающей жировой клетчатки.
При развитии изолированного перипанкреатического некроза сама ткань ПЖ может выглядеть так же, как при интерстициальном панкреатите.
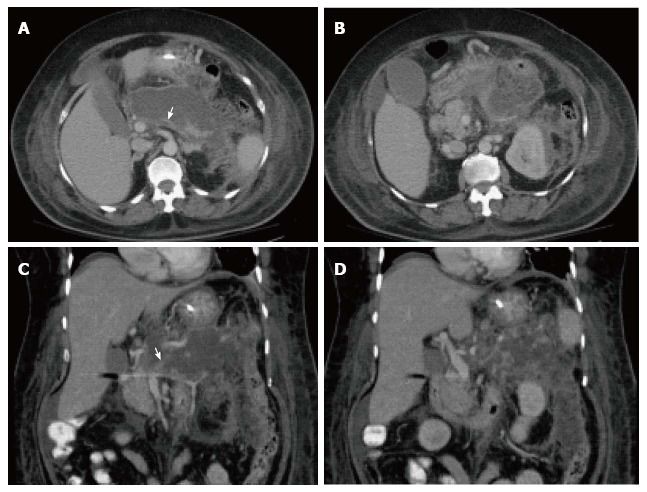
Рисунок 5 | Аксиальные (А, В) КТ-сканы в позднюю артериальную фазу контрастирования и их корональные (С, D) реконструкции.
Тело и хвост поджелудочной железы не накапливают контрастный препарат (полностью замещены некрозом). Гетерогенная область некроза и воспаления перипанкреатической жировой клетчатки. Стрелка указывает на тромбированную селезеночную вену (локальное осложнение процесса).
УЗИ:
При ОП одним из наиболее частых местных осложнений является образование жидкостных коллекторов; Атлантская классификация выделяет следующие их типы:
- жидкостное скопление, сопутствующее интерстициальному отечному панкреатиту
- острое перипанкреатическое скопление жидкости
- панкреатическая псевдокиста (формируется через 4 недели)
- жидкостное скопление, сопутствующее некротическому панкреатиту
- острое некротическое скопление
- отграниченный некроз (формируется через 4 недели)
Острое перипанкреатическое скопление жидкости
Может быть обнаружено в первые 4 недели от начала клинической картины. Выглядит как скопление гомогенного жидкостного содержимого без внутреннего солидного компонента. Оно ограниченно фасциальными пространствами брюшины и не имеет собственных стенок. Чаще всего локализуются в области малого сальника и переднем параренальном пространстве, однако могут «мигрировать» в области малого таза и средостения.
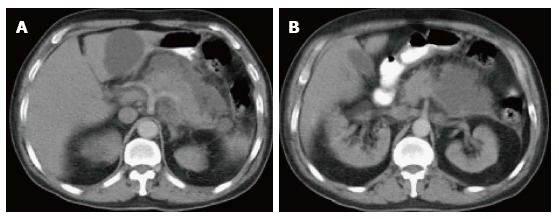
Рисунок 6 | На аксиальных КТ-сканах в портовенозную фазу поджелудочная железа слегка увеличена и несколько гетерогенно накапливает контрастное вещество.
Вентральнее железы можно увидеть скопление гомогенной жидкости без видимых стенок. Содержимое скопления не накапливает контраст. Эти признаки характерны для острого перипанкреатического скопления жидкости.
Около половины ОПСЖ формируется в первые 48 часов от начала процесса и разрешаются самостоятельно в течении месяца. При отсутствии осложнений и клинических проявлений не требуют хирургического вмешательства.
При КТ жидкостное содержимое низкой плотности (HU), на МР-томограммах — гиперинтенсивного сигнала в Т2 и гипоинтесивного (особенно заметно на фоне интенсивного сигнала от окружающей жировой клетчатки) — в Т1 и градиент-эхо.
Панкреатическая псевдокиста
О псевдокисте можно говорить через 4 недели от начала процесса — она представляет собой сохраняющееся скопление жидкости без солидного компонента, ограниченное четко определяемой стенкой.
При КТ стенки псевдокисты демонстрируют накопление контраста, больше выраженное в паренхиматозную фазу (что отражает присутствие грануляционной ткани). При МРТ же контрастное усиление можно заметить уже на ранних постконтрастных сканах, а своего пика оно достигает по прошествии около 5 минут после введения, что характерно для фиброзной ткани. Содержимое кисты не накапливает контраст.
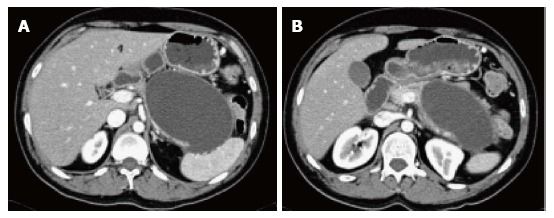
Рисунок 7 | Аксиальные КТ-сканы в позднюю портовенозную фазу контрастирования.
Определяется крупная овальной формы с четкими стенками псевдокиста, расположенная спереди тела и хвоста ПЖ, связанная с масс-эффектом на прилежащие отделы кишечника и ткань железы.
Иногда псевдокисты могут сообщаться с протоком поджелудочной железы, и обнаружение этой связи (при помощи МРХПГ) полезно для дальнейшего ведения пациентов.
Большинство псевдокист разрешаются спонтанно. Частым осложнением является инфицирование, которое может проявить себя наличием пузырьков газа. Однако отсутствие последних не исключает наличия осложнений; при клиническом подозрении стоит провести аспирационную биопсию содержимого.
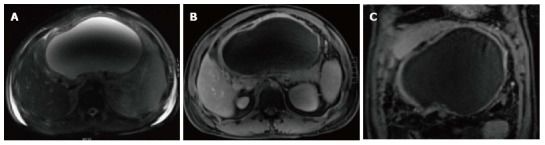
Рисунок 8
Аксиальные Т2 спин-эхо Т2ВИ (А), аксиальные и корональные постконтрастные 3D-GRE T1ВИ (В, С) демонстрируют наличие крупного жидкостного образования с четко определяемыми стенками (последние накапливают контрастное вещество) в области малого сальника. Содержимое гомогенное (гиперинтенсивная область в вентральных отделах обусловлена артефактом).
Диагноз: псевдокиста.
Острое некротическое скопление
Обнаруживается в первые 4 недели; важно помнить, что острое некротическое скопление может сопровождать только некротизирующий панкреатит. Некроз может вовлекать как паренхиму железы, так и перипанкреатическую клетчатку. Характерным КТ-признаком является наличие солидных компонентов в жидкостном скоплении; эти компоненты могут быть разных размеров и количества, а сами скопления могут быть как единичными, так и множественными.
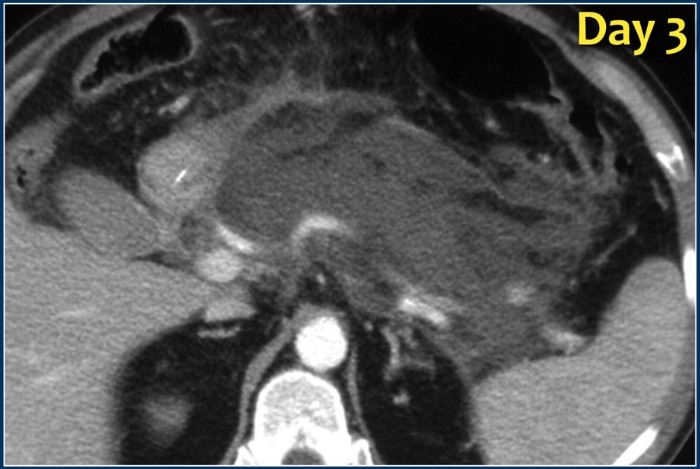
Рисунок 9
На аксиальном КТ-скане можно заметить скопление неоднородного жидкостного содержимого впереди от поджелудочной железы, большая часть паренхимы которой не накапливает контрастное вещество.
В первую неделю может быть сложно отличить некротическое скопление от перипанкреатического скопления жидкости — оба могут выглядеть как гомогенное жидкостное содержимое повышенной плотности; но по прошествии времени некротические включения становятся более заметными. МРТ и УЗИ также могут быть полезны для определения солидного содержимого.
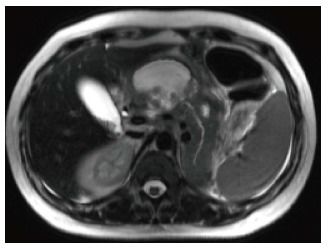
Рисунок 10 | Острое некротическое скопление.
Аксиальное турбо-спин-эхо Т2-взвешенное изображение. Впереди от поджелудочной железы определяется жидкостное скопление (гиперинтенсивного МР-сигнала), которое начинается от области шеи железы, которое сообщается с главным протоком железы. На фоне жидкостного содержимого можно увидеть включения низкого в Т2 сигнала — некротический детрит.
Отграниченный некроз
Формируется через 4 недели от начала процесса; является скоплением жидкости с солидными включениями, которое обязательно связано с некротизирующим панкреатитом и имеет сформированные стенки. Внутреннее солидное содержимое не накапливает контрастное вещество, стенки образования — накапливают так же, как и стенки псевдокисты.
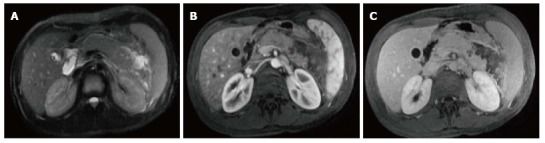
Рисунок 11 | Отграниченный некроз.
Аксиальные Т2 спин-эхо Т2ВИ (А), аксиальные и корональные постконтрастные 3D-GRE T1ВИ (В, С). В области перехода тела железы в хвост визуализируется область низкого в Т2 сигнала, которой на постконтрастных сканах соответствует зона нарушения перфузии. Также можно увидеть ограниченное стенкой скопление гетерогенного жидкостного содержимого.

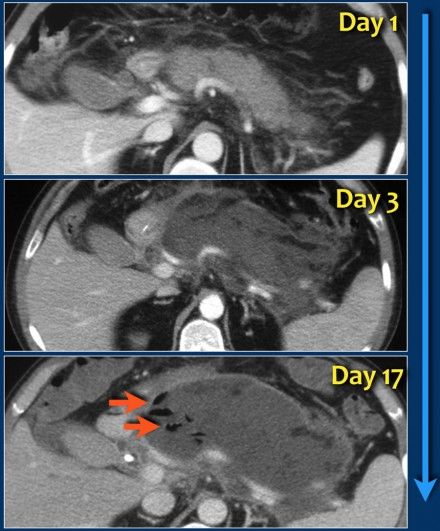
Рисунок 12 | Развитие инфицированного отграниченного некроза
На аксиальном постконтрастном КТ-скане, сделанном в первый день начала клинической картины железа выглядит диффузно увеличенной, окружающая жировая клетчатка тяжиста. При исследовании, проведенном на третий день вся ткань железы практически не накапливает контрастное вещество (некротизирующий панкреатит). На семнадцатый день можно увидеть сформированный, ограниченный стенкой коллектор с неоднородным содержимым, внутри которого визуализируются пузырьки газа (стрелка) — признак инфицированного некроза.
Тактика радиолога
Как уже было сказано, визуализация является необходимой для подтверждения диагноза ОП только если клинические и лабораторные данные сомнительны.
Однако лучевая картина в первые сутки от начала клинических проявлений может сбивать с толку: зачастую области некроза еще не успели сформироваться. Поэтому рентгенологу позволительно быть «ленивым» и не рекомендовать проведение КТ с контрастированием только что поступившему пациенту, а отложить процедуру (помните о лучевой нагрузке и возможных реакциях гиперчувствительности на контрастное вещество!). Наиболее четкая картина перфузионных нарушений формируется по прошествии недели от начала клинических проявлений
А вот в случаях, когда подозревается билиарный панкреатит, не стоит откладывать проведение МРХПГ, т.к. более ранняя экстракция конкремента улучшает прогноз для пациента.
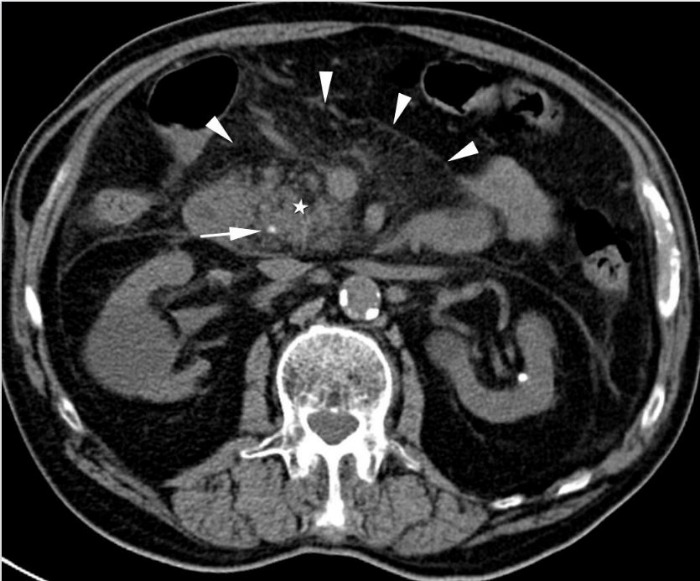
Рисунок 13 | Холедохолитиаз.
На нативном аксиальном КТ определяется плотный конкремент в общем желчном протоке на уровне головки ПЖ (звездочка). Тяжистость перипанкреатической жировой клетчатки говорит об интерстициальном панкреатите.
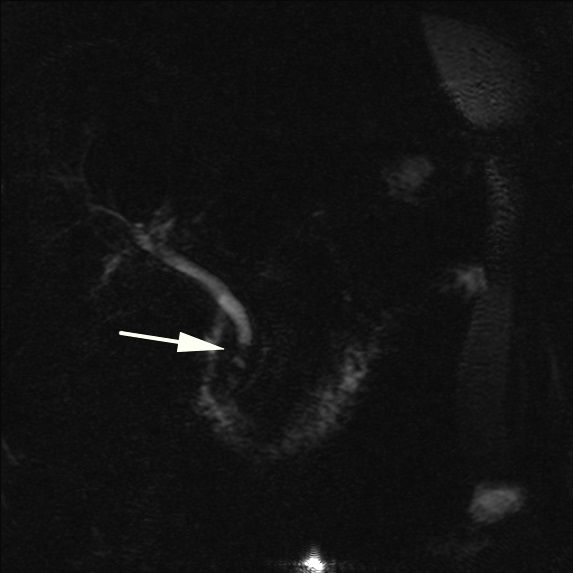
Рисунок 14
МРХПГ показала наличие конкремента в общем желчном протоке (стрелка, указывающая на дефект наполнения).
Источники
- Banks P. A. et al. Classification of acute pancreatitis—2012: revision of the Atlanta classification and definitions by international consensus //Gut. – 2013. – Т. 62. – №. 1. – С. 102-111.
- Федоровский В. В. СОВРЕМЕННАЯ МЕЖДУНАРОДНАЯ КЛАССИФИКАЦИЯ ОСТРОГО ПАНКРЕАТИТА-ОЧЕРЕДНОЙ ПЕРЕСМОТР //Journal of Siberian Medical Sciences. – 2015. – №. 3.
- Busireddy K. K. et al. Pancreatitis-imaging approach //World journal of gastrointestinal pathophysiology. – 2014. – Т. 5. – №. 3. – С. 252.
- O’Connor O. J., McWilliams S., Maher M. M. Imaging of acute pancreatitis //American Journal of Roentgenology. – 2011. – Т. 197. – №. 2. – С. W221-W225.
- Xiao B., Zhang X. M. Magnetic resonance imaging for acute pancreatitis //World journal of radiology. – 2010. – Т. 2. – №. 8. – С. 298.
- Олег Круглов. Радиография; Пересмотренная Атлантская классификация острого панкреатита – https://radiographia.info/article/peresmotrennaya-atlantskaya-klassifikaciya-ostrogo-pankreatita
- Thomas Bollen, Marieke Hazewinkel and Robin Smithuis. The radiology assistant; Pancreas – Acute Pancreatitis 2.0 – 2012 Revised Atlanta Classification of Acute Pancreatitis – https://www.radiologyassistant.nl/en/p550455dae5806/pancreas-acute-pancreatitis-20.html
- также по материалам ECR online 2018: W. Schima; Vienna. AT A-675 – A. Understanding the Atlanta 2012 classification of acute pancreatitis
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Источник
