Билиарнозависимый панкреатит клинические рекомендации
В статье рассматриваются основные причины возникновения острого и хронического билиарнозависимого панкреатита и особенности его лечения. Проанализирован клинический случай острого билиарного панкреатита, развившегося на фоне лечения желчнокаменной болезни, с дальнейшим формированием хронического панкреатита в результате персистирования билиарного сладжа.

Таблица 1. Клинический анализ крови
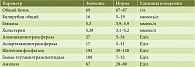
Таблица 2. Биохимический анализ крови
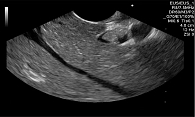
Замазкообразная желчь в терминальном отделе общего желчного протока
Как показали результаты ретроспективного (20-летний период) исследования, посвященного анализу причин развития острого панкреатита, билиарнозависимый панкреатит встречается у 26,9% пациентов [1]. Основной причиной его развития является желчнокаменная болезнь (ЖКБ). Острый панкреатит рассматривается как одно из основных осложнений ЖКБ [2].
Последние десятилетия во всем мире наблюдается тенденция к увеличению частоты развития билиарного панкреатита в результате роста заболеваемости ЖКБ [3]. Так, по данным разных авторов, частота развития билиарного панкреатита у больных ЖКБ составляет 25–90% [4].
Ведущим фактором в патогенезе билиарного панкреатита является повышение давления в желчных протоках вследствие возникновения механического препятствия (конкремент, билиарный сладж, стриктура, опухоль и др.), особенно дистальнее места слияния общего желчного с главным панкреатическим протоком, либо дисфункции сфинктера Одди. Развитие на этом фоне патологического билиопанкреатического рефлюкса и нарушение оттока панкреатического секрета могут привести к возникновению острого билиарного панкреатита [5].
Билиарнозависимый панкреатит отличается от панкреатита иной этиологии (алкогольный, алиментарный, посттравматический) тем, что этиологический фактор, как правило, не устраняется. Его воздействие продолжается на фоне развивающегося процесса в поджелудочной железе (ПЖ) и парапанкреатической клетчатке [6].
Особое значение в развитии билиарного панкреатита придается билиарному сладжу. Частота его выявления у больных с идиопатическим панкреатитом составляет 30–75%. При исследовании желчи в течение первых суток от начала панкреатической атаки билиарный сладж выявляется в 80% случаев [7].
В одном из исследований ученые наблюдали за 104 пациентами с билиарным сладжем в течение 630 дней (21 месяц). У 25 (24%) больных развились осложнения, такие как холелитиаз, холецистит, холедохолитиаз и панкреатит. При этом у 12 пациентов отмечался некалькулезный холецистит, у двоих – острый калькулезный холецистит. Зарегистрировано шесть случаев холецистолитиаза, один случай холедохолитиаза, четыре – панкреатита [8].
Таким образом, клиническое значение билиарного сладжа переоценить сложно, поскольку он:
- служит источником камнеобразования: желчные камни образуются у 5–20% пациентов за 1–3-летний период;
- способствует развитию стриктур терминального отдела общего желчного протока и/или стенозирующего папиллита;
- может приводить к развитию острого холецистита, холангита, отключению желчного пузыря (при наличии замазкообразной желчи);
- является причиной билиарного панкреатита.
Кроме того, билиарный сладж, содержащий микролиты, может свободно проходить по протоковой системе и вызывать необъяснимые боли в правом подреберье у 83% больных [9].
Билиарный сладж формируется в желчном пузыре в результате дестабилизации физико-химического состояния желчи и преципитации ее основных компонентов.
К факторам, способствующим персистенции билиарного сладжа, относятся гипотония желчного пузыря и гипертонус сфинктера Одди. Постоянный пассаж сладжа по желчным путям приводит к повреждению слизистой оболочки, главным образом в области сфинктера Одди. Травматизация слизистой оболочки вызвана микролитами, составляющими основную часть билиарного сладжа. Как следствие, сначала развивается вторичная дисфункция сфинктера Одди, затем формируется стенозирующий папиллит [4].
Помимо конкрементов и билиарного сладжа обострения панкреатита могут быть вызваны дисфункцией сфинктера Одди [10], в том числе у больных после холецистэктомии [11]. Так, у 18,8% пациентов с хотя бы одним эпизодом острого панкреатита или хроническим идиопатическим панкреатитом выявляется панкреатический тип дисфункции сфинктера Одди [11].
Фармакотерапия билиарнозависимого панкреатита может быть этиологической и патогенетической. При наличии показаний (ЖКБ, обструкция желчного потока) проводится эндоскопическое или хирургическое лечение.
Этиологическая терапия предполагает использование препаратов урсодезоксихолевой кислоты (УДХК). Патогенетическая зависит от типа преобладающих нарушений. При гипомоторных нарушениях назначают прокинетики (домперидон, итоприд), при гипермоторных – спазмолитики (мебеверин). Применяют также комбинированные препараты, оказывающие одновременно и холеретическое, и спазмолитическое действие.
По механизму действия спазмолитики подразделяют на нейротропные и миотропные. Нейротропные блокируют процесс передачи нервных импульсов в вегетативных ганглиях и нервных окончаниях, стимулирующих гладкомышечные клетки. Они осуществляют блокаду М1-, М2- и М3-холинорецепторов гладкой мышечной клетки. Среди нейротропных спазмолитиков выделяют:
- природные: атропин, гиосциамин, препараты красавки, платифиллин, скополамин;
- синтетические центральные: адифенин, апрофен, апринал, циклозил;
- полусинтетические периферические: гиосцина бутилбромид.
Миотропные спазмолитики уменьшают мышечный тонус за счет прямого воздействия на гладкомышечные клетки. К таким спазмолитикам относятся блокаторы ионных каналов, ингибиторы фосфодиэстеразы (ФДЭ) 4-го типа, нитраты. Миотропные спазмолитики подразделяют:
- на селективные:
- блокаторы кальциевых каналов (пинаверия бромид, отилония бромид);
- блокаторы натриевых каналов (мебеверин) и донаторы оксида азота (изосорбида динитрат, нитроглицерин, натрия нитропруссид);
- неселективные: ингибиторы ФДЭ (дротаверин, папаверин, аминофиллин, бенциклан) [12].
Что касается патогенетической терапии, препаратом выбора для пациентов с функциональными заболеваниями билиарного тракта являются лекарственные средства, селективно релаксирующие гладкую мускулатуру органов желудочно-кишечного тракта. Препараты этой группы, в частности мебеверин, обладают релаксирующей селективностью в отношении сфинктера Одди, в 20–40 раз превышающей эффект папаверина. При этом мебеверин оказывает нормализующее действие на мускулатуру кишечника, устраняя функциональный дуоденостаз, гиперперистальтику, спазм и не вызывая при этом нежелательной гипотонии [13].
Рассмотрим клинический пример, демонстрирующий результат успешного лечения билиарнозависимого панкреатита за счет назначения этиологической и патогенетической терапии.
Больная К. 76 лет была госпитализирована в отделение патологии поджелудочной железы и желчевыводящих путей Московского клинического научно-практического центра им. А.С. Логинова для обследования и лечения по поводу неоднократного обострения хронического панкреатита.
При поступлении – жалобы на боли в верхней половине живота с иррадиацией в спину и грудную клетку, усиливающиеся после еды, тошноту, отрыжку, снижение массы тела на 16 кг за два года.
Из анамнеза известно, что боли в животе впервые появились несколько лет назад. Больная была госпитализирована с болевым синдромом. Диагностированы холедохолитиаз, механическая желтуха. Проведены эндоскопическая папиллосфинктеротомия, экстракция конкремента холедоха, осложнившаяся панкреонекрозом. Проведено консервативное лечение. Через полгода отмечалось повторное ухудшение – интенсивный болевой синдром. Пациентка была вновь госпитализирована. Диагноз: хронический панкреатит, обострение. Через два года выполнена лапароскопическая холецистэктомия. В течение года боли не беспокоили, однако через год они возобновились. Последующие полгода пациентка с диагнозом «обострение хронического панкреатита, транзиторный холедохолитиаз» находилась на стационарном лечении.
При объективном осмотре состояние удовлетворительное, кожные покровы и видимые слизистые оболочки чистые, обычной окраски. Тургор снижен. Отеков нет. В легких дыхание везикулярное, хрипов нет. Тоны сердца приглушены, ритм правильный. Частота сердечных сокращений – 76 уд/мин. Артериальное давление – 120/80 мм рт. ст. Язык влажный, обложен белым налетом. Живот обычной конфигурации, в эпигастральной области и правом подреберье звездчатые рубцы. При пальпации живот мягкий, болезненный в эпигастральной области. Печень у края реберной дуги, селезенка не пальпируется.
Лабораторно-инструментальные исследования. Клинический анализ крови без патологических отклонений (табл. 1). В биохимическом анализе крови умеренный холестаз (табл. 2). Фекальная эластаза – свыше 200 мкг/г. Эзофагогастродуоденоскопия. Парапапиллярный дивертикул. Состояние после папиллотомии.
Ультразвуковое исследование органов брюшной полости. Признаки диффузного заболевания печени. Билиарная гипертензия. Расширение гепатикохоледоха. Не исключен холедохолитиаз, хотя конкремент не визуализируется. Диффузные изменения поджелудочной железы (признаки хронического панкреатита).
Для определения дальнейшей тактики лечения выполнена эндосонография панкреатобилиарной зоны. Визуализирована замазкообразная желчь в общем желчном протоке (рисунок).
Вероятно, именно замазкообразная желчь в терминальном отделе общего желчного протока стала причиной частых обострений хронического билиарнозависимого панкреатита.
Для уменьшения литогенности желчи больной назначили препарат УДХК Эксхол® 500 мг в делимых таблетках в дозе 750 мг/сут в три приема. Благодаря такой форме выпуска Эксхол® 500 мг можно гибко дозировать, сокращая количество принимаемых таблеток [14]. При выборе препаратов УДХК это очень важно. Не менее значимый фактор – экономическая составляющая. Выбор препарата в рассматриваемом случае был обусловлен доступностью длительного курсового лечения.
С целью купирования болевого синдрома, устранения спазма и улучшения пассажа желчи в кишку был назначен Спарекс® по 200 мг в два приема перед едой. Через три месяца лечения отмечалась положительная динамика в виде полного купирования болевого синдрома, нормализации биохимических показателей. Наблюдение за больной в последующие шесть месяцев показало отсутствие рецидивов билиарнозависимого панкреатита.
По данным Н.А. Агафоновой и соавт. [14], российский препарат мебеверина Спарекс® не только купирует боль, но и улучшает реологические свойства желчи при ЖКБ.
Оценка безопасности и переносимости мебеверина проводилась в исследованиях, включивших свыше 3500 больных [13]. Во всех исследованиях отмечалась хорошая переносимость препарата без развития побочных эффектов, в том числе при увеличении дозы. Мебеверин не вызывает гематологических и биохимических изменений, не оказывает типичных антихолинергических эффектов, в связи с чем может назначаться пациентам с гипертрофией предстательной железы и глаукомой [13], что актуально для пожилых больных.
Таким образом, несмотря на проведенную папиллосфинктеротомию, отток желчи был нарушен, что в свою очередь провоцировало обострения хронического панкреатита. Данных о формировании стриктур не получено. В связи с этим хирургическое вмешательство было нецелесообразным. Ситуация была разрешена путем применения препарата УДХК (Эксхол®) и селективного миотропного спазмолитика (Спарекс®).
Источник
Панкреатит является клиническим диагнозом, который определяется воспалением поджелудочной железы. Несмотря на то, что заболевание не всегда клинически различимо, выделяют острый и хронический панкреатит.
Острый панкреатит является самоограничивающимся и обратимым повреждением поджелудочной железы, которое ассоциируется с болью в срединной области эпигастрия, а также повышенным уровнем панкреатических ферментов в сыворотке крови, тогда как хронический панкреатит характеризуется рецидивной или постоянной болью в животе, а также прогрессивным повреждением поджелудочной железы и окружающих структур, что приводит к образованию рубцов и потере функции.
У пациентов с рецидивирующими приступами панкреатита выявление причины и типа панкреатита предусматривает дифференциацию среди 4 следующих типов:
- Рецидивирующий острый панкреатит: возможна идентификация причины острого панкреатита, которая не приводит к развитию хронического панкреатита (например, желчные камни, лекарственные препараты, гиперкальциемия и т.д.)
- Идиопатический панкреатит: исчерпывающее исследование не позволяет выявить причину. Наиболее часто это хронический рецидивирующий панкреатит или четко выраженный хронический панкреатит.
- Хронический рецидивирующий панкреатит: пациенты страдают от хронической боли, которая не распознается клинически как хронический панкреатит (нет отличительных особенностей), однако наблюдаются патологические изменения в образцах ткани.
- Установленный хронический панкреатит: присутствуют отличительные особенности хронического панкреатита, в частности уменьшенная экзокринная функция поджелудочной железы, нарушение всасывания, диабет, а также кальцификаты поджелудочной железы.
ЭТИОЛОГИЯ
Основными причинами хронического панкреатита в мире являются алкоголь (70–80%), идиопатический хронический панкреатит и другие причины. Подобным образом, около 70% случаев хронического панкреатита на западе связаны с алкоголем, однако последние одноцентровые и многоцентровые исследования в США зафиксировали частоту 51% и ниже. Патологоанатомические исследования показывают, что хронический панкреатит в 45–50 раз чаще встречается у людей с алкоголизмом.
Неизвестно, есть ли непрерывный спектр индивидуальных пороговых значений токсичности алкоголя или же абсолютное пороговое значение, поскольку имеющиеся данные неоднозначны. Наблюдения в ходе метаанализа подтверждают линейную взаимосвязь между дозой алкоголя и риском панкреатита у мужчин, в то же время нелинейную взаимосвязь у женщин, при этом последнее, вероятно, вызвано включением лиц, ранее страдавших алкоголизмом, в контрольную группу.
Публикуются данные небольших исследований о том, что логарифм среднего дневного потребления алкоголя линейно коррелирует с риском развития хронического панкреатита. Большинство пациентов сообщают, что употребляют от 150 г алкоголя в день на протяжении многих лет, однако риск развития хронического панкреатита увеличивается при употреблении всего лишь 25 г алкоголя или более в день (около 2-х порций спиртных напитков). В отличие от этого, в ходе большого многоцентрового исследования было установлено, что только тяжелое злоупотребление алкоголем (5 или более порций спиртных напитков в день) существенно увеличивает риск развития хронического панкреатита. Вместе с тем, лишь у немногих лиц, злоупотребляющих алкоголем, развивается хронический панкреатит (не более 10%, возможно <3%), а также общее потребление алкоголя лицами, которые им злоупотребляют, при хроническом панкреатите по сравнению с его отсутствием не увеличено. Это свидетельствует в пользу того, что для существенного уменьшения порогового количества алкоголя, необходимого для развития хронического панкреатита, требуется воздействие кофакторов.
К ним относятся:
- табакокурение,
- диета с высоким содержанием жиров/белков,
- генетическая предрасположенность (например, полиморфизм гена 5′-дифосфоглюкуронозилтрансферазы),
- возможно инфекции Коксаки.
В то же время, было показано, что употребление кофе снижает риск развития алкогольного хронического панкреатита у курящих лиц.
ПАТОФИЗИОЛОГИЯ
Пусковые факторы, пороговые значения, иммунологический ответ, а также клеточные механизмы хронического панкреатита остаются до конца не исследованными. К традиционным концепциям, объясняющим патогенез хронического панкреатита, относят: окислительный стресс, токсикометаболические факторы, обструкцию проток, а также некроз и фиброз.
Согласно гипотезе первичного вовлечения протока предполагается, что первый приступ начинается в протоках поджелудочной железы как первичная аутоиммунная или воспалительная реакция, тогда как гипотеза сигнального острого панкреатита указывает на то, что первый приступ затрагивает ацинарные клетки, что запускает изолирование воспалительных клеток и секрецию цитокинов.
Удаление пускового фактора(-ов) приводит к заживлению, но при постоянной секреции цитокинов фиброгенные звездчатые клетки поджелудочной железы секретируют коллаген и запускают развитие фиброза и хронического панкреатита. Однако возможность влияния на естественное протекание хронического панкреатита не установлена, поскольку устранение основных факторов риска, таких как алкоголь, не приводит к обратному развитию заболевания.
Механизмы боли при хроническом панкреатите не определены, но, скорее всего, являются следствием многих причин, в частности, воспаления поджелудочной железы, связанных с фиброзом повышений давления внутри поджелудочной железы и ее ишемии, нервных источников боли (воспаление оболочки нерва, фиброзное обрастание чувствительных нервов, нейропатия), а также могут быть вызваны причинами, не связанными с поджелудочной железой (например, стеноз общего желчного протока, дуоденальный стеноз, псевдокисты поджелудочной железы). Основной акцент актуального исследования направлен на нейропатическое происхождение боли.
КЛАССИФИКАЦИЯ
Классификация Сальса
Сальс классифицировал хронический панкреатит на 3 основные группы:
- Обструктивный панкреатит
- Воспалительный панкреатит
- Литогенный или кальцифицирующийся хронический панкреатит.
Классификация TIGAR-O
Этиологическая классификация хронического панкреатита TIGAR-O объединяет сведения относительно генетических, экологических, иммунологических, патобиологических факторов риска, ассоциированных с хроническим панкреатитом. Этиологическая классификация TIGAR-O предусматривает 6 групп хронического панкреатита:
1. Токсико-метаболический
- Алкоголизм
- Табакокурение
- Гиперкальциемия
- Гиперлипидемия
- Хроническое заболевание почек
- Лекарства: злоупотребление фенацетином (слабая связь)
- Токсины: оловоорганические компоненты, например, ди-N-бутилтиндихлорид (ДБТХ)
2. Идиопатический
- С ранним началом
- С поздним началом
- Тропический
3. Генетический
- Наследственный панкреатит: мутации катионного трипсиногена
- Мутации муковисцидозного трансмембранного регулятора проводимости (CFTR)
- Мутации ингибитора сериновой протеазы Kazal типа 1 (SPINK1)
- Мутации хемотрипсиногена С (CTRC)[
- Мутации кальций-чувствительного рецептора (CaSR, CSR)
- Мутации клаудина-2 (CLDN2)
- Карбоксипептидаза Aс1 (CPA1)
- Фукозилтрансфераза 2 (FUT2) несекреторного статуса
- Группа крови B (III) по системе ABO
4. Аутоиммунный
- Изолированный аутоиммунный хронический панкреатит
- Симптоматический аутоиммунный хронический панкреатит связан с синдромом Шегрена, воспалительным заболеванием кишечника, первичным билиарным циррозом печени
5. Рецидивирующий и тяжелый острый панкреатит
- Пост-некротический (тяжелый острый панкреатит)
- Рецидивирующий острый панкреатит
- Сосудистые заболевания/ишемия
- Возникающий после облучения
6. Обструктивный
- Разделённая поджелудочная железа (неоднозначно)
- Дисфункции сфинктера Одди (неоднозначно)
- Обструкция протока (например, солидной опухолью, внутрипротоковой папиллярномуцинозной опухолью)
- Периампулярные кисты стенки двенадцатиперстной кишки
- Посттравматические рубцы протоки поджелудочной железы.
ПОШАГОВЫЙ ДИАГНОСТИЧЕСКИЙ ПОДХОД
Установление диагноза может быть затруднено. Индивидуальные симптомы пациента, а также объективная диагностика сами по себе указывают на возможность хронического панкреатита, однако постановка диагноза, как правило, требует объединения всех признаков. Было предложено несколько диагностических критериев, но ни один из них не принят в качестве универсального. У пациентов с поздней манифестацией заболевания необходимо рассмотреть возможность развития аутоиммунного панкреатита и рака поджелудочной железы, которые необходимо исключить как дифференциальные диагнозы, что может составить трудность.
Диагностика хронического панкреатита на ранних стадиях также является затруднительной, если из признаков отмечается только боль, а результаты диагностических исследований с визуализацией являются неинформативными. В данном случае требуется проспективное наблюдение за пациентом.
Например, после первого приступа острого панкреатита у 8–10% пациентов может развиваться хронический панкреатит; прогрессирование независимо прогнозировано четырьмя переменными: курение в настоящее время, идиопатическая этиология, алкогольная этиология и некротизирующий панкреатит. Более того, в трех продолжительных исследованиях отмечается, что у 26–50% пациентов с идиопатическими приступами (рецидивирующие приступы неустановленной этиологии) признаки хронического панкреатита развиваются на протяжении 1,5–3 лет.
Клинические признаки
Отличительными клиническими признаками являются:
- Боль в животе: наблюдается более, чем у 80% пациентов на момент постановки диагноза. Боль локализуется в эпигастрии, притупленная, отдает в спину, ослабляется в положении сидя вперед, усиливается приблизительно через 30 минут после приема пищи.
- Желтуха: общая частота данного симптома составляет около 10%. Является следствием сдавления общего желчного протока и, как правило, характеризуется предварительным повышением уровня щелочной фосфатазы без желтухи или каких-либо других симптомов. Если присутствует данный симптом, необходимо исключить развитие злокачественного новообразования.
- Стеаторея: общая частота колеблется в пределах от 8 до 22% на момент постановки диагноза. Стеаторея возникает перед азотореей (нарушением всасывания пищевого белка). Это происходит вследствие повреждения, атрофии и потери экзокринной ткани поджелудочной железы в результате воспаления и фиброза железы. Если присутствует данный симптом, необходимо исключить употребление минеральных масел.
- Недоедание: как правило развивается в результате боязни употреблять еду (вследствие боли), мальабсорбции, уменьшения количества употребляемой еды, связанного со злоупотреблением алкоголем, а также увеличенного потребления энергии в состоянии покоя у 30–50% пациентов. Для 10-15% пациентов потребуется применение пищевых добавок.
- Сахарный диабет и нарушение толерантности к глюкозе: нарушение толерантности к глюкозе возникает на раннем этапе вследствие инсулинорезистентности, а позже развивается сахарный диабет в результате инсулинопении. Общая распространенность гипергликемии составляет 47%. Частота сахарного диабета варьирует в пределах 0–22% на момент манифестации симптомов, а также более 80% после 25 лет. В проспективном когортном исследовании у 500 пациентов были выявлены два независимых фактора риска (кальцификаты поджелудочной железы и дистальная резекция поджелудочной железы), однако в значительно большем ретроспективном исследовании у свыше 2000 пациентов были выявлены 5 независимых факторов риска, среди которых не было кальцификатов (алкоголизм, мужской пол, стеаторея, стеноз желчного протока и дистальная панкреатэктомия).
Среди неспецифических клинических признаков выделяют:
- Потерю веса: как и при недоедании, это является следствием боязни употреблять еду (вследствие боли), мальабсорбции, уменьшения количества употребляемой еды, связанного со злоупотреблением алкоголем, а также увеличенного потребления энергии в состоянии покоя. Вместе с тем, необходимо исключить злокачественное новообразование.
- Дефицит питательных микроэлементов: как и при недоедании, это является следствием боязни употреблять еду (вследствие боли), мальабсорбции, уменьшения количества употребляемой еды, связанного со злоупотреблением алкоголем, а также увеличенного потребления энергии в состоянии покоя. Распространенность дефицита жирорастворимых витаминов отличается, для витамина А регистрируется на уровне 14,5%, для витамина Е – 24,2%, для витамина D – на уровне 53%. Эти дефициты могут потенциально в долгосрочной перспективе привести к проблемам со здоровьем, в частности, к расстройствам зрения, неврологическим нарушениям, а также ухудшению состояния костей.
- Переломы костей при незначительной травме и уменьшенная минеральная плотность костей: как и при недоедании, это связано с дефицитом питательных микроэлементов и увеличенным системным воспалением. Распространенность перелома костей при незначительной травме зафиксирована на уровне 4,8%, возможно вследствие высокой распространенности остеопении (39,8%) и остеопороза (23,4%). Риск перелома более высок, если алкоголь является основным фактором риска развития хронического панкреатита и у пациента наблюдается цирроз.
- Тошнота и рвота: происходит из-за краткосрочных и долгосрочных осложнений хронического панкреатита. Может быть результатом боли, обструкции желчных проток или двенадцатиперстной кишки, а также изменений миоэлектрической активности желудка после приема пищи и усугубляется в случае приема наркотических анальгетиков. Вместе с тем, нет единого мнения в отношении того, имеют пациенты с хроническим панкреатитом замедленное, нормальное или быстрое опорожнение желудка.
- Кожные узелки: липаза поджелудочной железы может попадать в кровоток и приводить к адипонекрозу в других тканях. Это приводит к появлению болезненных и безболезненных кожных узелков на конечностях, которые ассоциируются с лихорадкой и полиартритом. Около 5% пациентов с панкреатитом характеризуются развитием интрамедуллярного адипонекроза, но, как правило, это не проявляется какими-либо симптомами.
- Болезненные суставы: симптом возникает как минимум при 2-х состояниях, связанных с болезнью поджелудочной железы: метастатическом адипонекрозе и связанном с иммуноглобулином G4 (IgG4) аутоиммунном панкреатите, ассоциированном с ревматоидным артритом с или без вторичного амилоидоза.
- Вздутие живота: происходит вследствие появления увеличенных псевдокист, рака поджелудочной железы, панкреатического асцита в результате выхода жидкости из разрушенного протока или псевдокисты, а также дуоденального фиброза и обструкции, которые приводят к растяжению желудка.
- Одышка: вследствие плеврального выпота, вторично связанного сомвыхода жидкости из разрушенного протока или псевдокисты, и ее попаданием в плевральную полость.
Возраст на момент манифестации указывает на основную этиологию. Наследственный панкреатит наиболее часто проявляется в возрасте 10–14 лет, ювенильный идиопатический хронический панкреатит – 19–23 лет, алкогольный хронический панкреатит – 36–44 года, сенильный идиопатический хронический панкреатит – 56–62 года.
Источник
