Детоксикация при деструктивном панкреатите
1. Мороз В.В., Григорьев Е.В., Чурляев Ю.А. Абдоминальный сепсис. М.; 2006: 192.
2. Багненко С.Ф., Толстой А.Д., Краснорогов В.Б., Курыгин А.А., Синенченко Г.И., Сухарев В.Ф., Гринёв М.В., Лапшин В.Н., Вербицкий В.Г., Киселёв В.А., Кабанов М.Ю., Гольцов В.Р. Острый панкреатит. Протоколы диагностики и лечения. Санкт-Петербургский НИИ скорой помощи им. И.И. Джанелидзе. СПб.; 2004: 12.
3. Ермолов А.С., Иванов П.А., Беляев А.А. Роль малоинвазивных вмешательств при лечении острого панкреатита. Мат-лы городского семинара. М.: НИИ скорой помощи им. Н.В. Склифосовского; 2003: 5—9.
4. Гостищев В.К., Глушко В.А. Панкреонекроз и его осложнения. Основные принципы хирургической тактики. Хирургия. Журн. им. Н.И.Пирогова. 2003; 3: 50—54. PMID: 12698653
5. Горский В.А., Ковальчук Л.В., Агапов М.А., Хорева М.В., Ованесян Э.Р., Никонова А.С., Греченко В.В. Антимедиаторная терапия в комплексном лечении острого деструктивного панкреатита. Хирургия. Журн. им. Н.И.Пирогова. 2010; 3: 54—61. PMID: 20524238
6. Beger H.G., Rau B., Isenmann R. Natural history of necrotizing pancreatitis. Pancreatology. 2003; 3 (2): 93-101. https://dx.doi.org/10.1159/000070076. PMID: 12774801
7. Попова Е.Ю., Кузнецов H.A., Владимиров В.Г., Заринская С.А., Андрейцев А.Н., Бронтвейн А.Т., Кузин А.Н. Поражение забрюшинной клетчатки при деструктивном панкреатите. Хирургия. Журн. им. Н.И.Пирогова. 2004; 8: 52—55. PMID: 15340319
8. Buter A., Imrie C.W., Carter C.R., Evans S., McKay C.J. Dynamic nature of early organ dysfunction determines outcome in acute pancreatitis. Br. J. Surg. 2002; 89 (3): 298—302. https://dx.doi.org/10.1046/j.0007-1323.2001.02025.x. PMID: 11872053
9. Филимонов М.И., Гельфанд Б.Р., Бурневич С.З. Деструктивный панкреатит: комплексная диагностика и лечение. Новый мед. журнал. 1997; 4 (3): 10—13.
10. Хорошилов С.Е., Никулин А.В. Эфферентное лечение критических состояний. Общая реаниматология. 2012; 8 (4): 30—41. https://dx.doi.org/10.15360/1813-9779-2012-4-30
11. Хорошилов С.Е., Никулин А.В., Марухов А.В. Предупреждение развития синдрома полиорганной недостаточности в ферментативной фазе тяжелого острого панкреатита. Вестн. НМЦХ им. Н.И.Пирогова. 2014; 9 (1): 58—62.
12. Гуменюк Н.И., Киркилевский С.И. Инфузионная терапия. Теория и практика. Киев: Книга плюс; 2004: 119—123.
13. Кравец В.П., Кравец В.В. Диагностика и лечение больных с парезом кишечника в раннем послеоперационном периоде. Вестн. Сумского Государственного университета. Серия: Медицина. 2007; 2: 172—175.
14. Батоцыренов Б.В., Ливанов Г.А., Андрианов А.Ю., Васильев С.А., Кузнецов О.А. Особенности клинического течения и коррекция метаболических расстройств у больных с тяжелыми отравлениями метадоном. Общая реаниматология. 2013; 9 (2): 18—22. https://dx.doi.org/10.15360/1813-9779-2013-2-18
15. Еремеева Л.Ф., Менщиков В.В., Бердников А.П., Ямпольский А.Ф. Проведение липидной «он лайн» гемодиафильтрации (экспериментальное исследование). Общая реаниматология. 2013; 9 (1): 37—42. https://dx.doi.org/10.15360/1813-9779-2013-1-37
16. Корнилов И.А., Гражданкин И.О., Редькин Д.А., Дерягин М.Н., Ефремов С.М., Ломиворотов В.В. Экстракорпоральная мембранная оксигенация при остром инфаркте миокарда, осложнённом кардиогенным шоком. Общая реаниматология. 2013; 9 (3): 54—57. https://dx.doi.org/10.15360/1813-9779-2013-3-54
17. Хорошилов С.Е., Никулин А.В., Марухов А.В. Применение плазмафереза в ферментативной фазе тяжелого острого панкреатита. Общая реаниматология. 2013; 9 (6): 53—60. https://dx.doi.org/10.15360/1813-9779-2013-6-53
Источник
 Острый деструктивный панкреатит
Острый деструктивный панкреатитОстрый деструктивный панкреатит представляет собой один из тяжелейших недугов, которые встречаются у человека при расстройствах функционирования поджелудочной.
Панкреатиты представляют собой комплекс недугов, при которых фиксируется появление и развитие острого воспаления в тканях органа, сопровождающееся возникновением деструктивных процессов, связанных с патразрушением структуры и целостности клеток железы. В процессе прогрессирования острого деструктивного панкреатита клеточной мембраны наблюдается заполнение свободного межклеточного пространства ферментами, синтезируемыми клетками поджелудочной, что вызывает самопереваривание тканей.
Общая характеристика и фазы прогрессирования острой деструктивной формы панкреатита
В случае прогрессирования в 15-20% случаев болезнь приобретает деструктивные формы острого панкреатита. При развитии острой формы деструктивного панкреатита смертность составляет до 30% случаев. В случае развития тяжелой формы недуга летальность может достигать 100%.
При остром деструктивном панкреатите максимальная летальность наблюдается в первую, третью и четвертую недели с момента начала развития заболевания в организме. Смерть пациента при остром деструктивном панкреатите на второй неделе прогрессирования недуга фиксируется реже всего. Летальный исход на этой стадии характерен для людей в пожилом возрасте. Неблагоприятный исход на второй неделе течения заболевания может наступить в случае развития недуга у человека с ослабленным организмом.
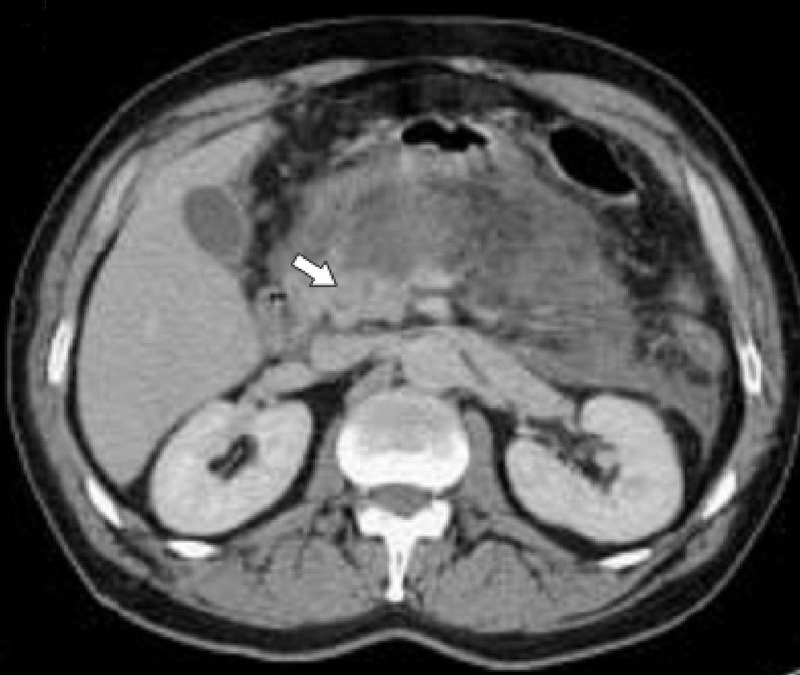 Компьютерная томография деструктивного панкреатита
Компьютерная томография деструктивного панкреатита
При прогрессировании острой формы деструктивного панкреатита выделяются несколько фаз, для которых характерно проявление определенных изменений в тканях поджелудочной и тканях, окружающих орган.
Фазы заболевания:
- Первая фаза острого деструктивного панкреатита носит название ферментативной. Длительность этой фазы составляет до 3 суток с момента начала развития болезни, при этом наблюдается формирование участков некроза тканей поджелудочной. В конце ферментативной фазы наблюдается светлый промежуток, при котором происходит снижение проявлений симптомов болезни и переход ферментативной фазы в реактивную.
- Вторая фаза острой формы деструктивного панкреатита носит название реактивной, как правило, эта фаза недуга регистрируется со второй недели развития нарушения. Реактивная фаза является промежуточной и носит название фазы перипанкреатического инфильтрата.
- Третья фаза острого деструктивного панкреатита носит название стадии секвестрации. Эта фаза развивается с третьей недели течения болезни.
Третья фаза острого деструктивного панкреатита в своем прогрессировании может иметь 3 типа развития событий.
Первое направление характеризуется процессом рассасывания перипанкреатического инфильтрата и наступлением выздоровления пациента, такое течение недуга наблюдается в 35% случаев выявления болезни.
У 1/3 пациентов, заболевших острым деструктивным панкреатитом, наблюдается прогрессирование асептической секвестрации, которая заключается в осуществлении процесса отторжения некротизированного участка от тканей органа, сохранивших свою жизнеспособность. В случае развития недуга в этом направлении происходит формирование парапанкреатической кисты без нагноений.
У 30-35% пациентов наблюдается прогрессирование септической секвестрации, при которой происходит формирование гнойных и септических осложнений. Этот вариант третьей фазы является наиболее опасным для здоровья и жизни человека.
Причины и симптоматика развития острой формы деструктивного панкреатита
В соответствии с данными, полученными в результате научных исследований, которые проведены в последнее время, основными факторами острого деструктивного панкреатита являются:
- алкогольсодержащие напитки;
- недуги, связанные с нарушениями в работе желчевыводящих путей;
- заражение глистами;
- травмы брюшины;
- интоксикации различного генеза.
 При первых подозрениях на панкреатит пациента следует немедленно госпитализировать
При первых подозрениях на панкреатит пациента следует немедленно госпитализировать
При наличии соответствующего опыта любой медик без особых трудностей способен выявить у пациента прогрессирование острого деструктивного панкреатита. Заболевание легко определяется по наличию триады признаков:
- Сильные боли в области эпигастрия.
- Возникновение регулярных рвотных позывов.
- Сильный метеоризм.
Болевые ощущения чаще всего возникают внезапно и имеют высокую интенсивность и силу, очень часто наблюдаются при употреблении жирной пищи или алкоголя при остром деструктивном панкреатите. Болевые ощущения могут сопровождаться шоком, потерей сознания и частыми рвотными позывами. Частая и изнуряющая рвота ведет к прогрессированию обезвоживания.
Помимо указанных признаков у человека наблюдаются симптоматика, характерная для общей интоксикации – это повышение температуры тела, возникновение озноба, тахикардии, одышки и цианоза слизистых оболочек организма больного.
Особенности ощущаемых болей находятся в полной зависимости от формы недуга и причин его возникновения. Основными особенностями проявлениями болей считаются следующие:
- возникновение дискомфортных ощущений;
- впадение пациента в состояние коллапса;
- развитие острых болей в области эпигастрия;
- появление нестерпимых болевых ощущений.
Возникающая в процессе прогрессирования болезни рвота не приносит облегчения пациенту. Кожные покровы лица при этом приобретают красный оттенок, а при впадении человека в коллапс наблюдается побледнение кожного покрова.
Прогрессирующее заболевание приводит к повышению концентрации эластазы, которая провоцирует запуск процесса разрушения сосудов кровеносной системы, что приводит к возникновению кровотечений в органах, входящих в систему пищеварения.
Методики диагностирования острого деструктивного панкреатита у пациента
Важно! Для того чтобы лечение было максимально эффективным, необходимо оперативно и точно поставить диагноз.
При проведении диагностики заболевания особое внимание следует обращать на пациентов, которые имеют функциональные нарушения в работе поджелудочной.
При первых подозрениях на панкреатит пациента следует немедленно госпитализировать.
Внимание! Сложность заболевания заключается в том, что нарушения, возникающие в организме, способны очень быстро спровоцировать развитие коматозного состояния и других опасных для организма состояний.
Для выявления патологических изменений применяется ультразвуковое обследование пациента, которое позволяет выявить:
- наличие отека поджелудочной;
- прогрессирование некротических процессов;
- неравномерность структуры тканей органа.
 УЗИ брюшной полости позволяет выявить изменения в тканях поджелудочной
УЗИ брюшной полости позволяет выявить изменения в тканях поджелудочной
Помимо УЗИ применяются компьютерная томография и цилиакография.
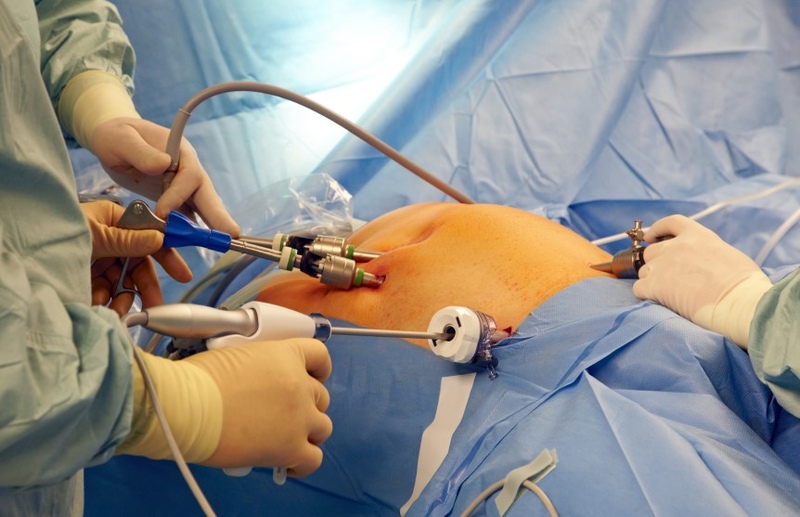
Наиболее информативным методом обследования является лапароскопия. Применение этого метода позволяет провести дифференциацию диагноза, отличить панкреонекроз от холецистита, прободной язвы и некоторых других острых состояний организма, связанных с нарушениями в работе органов брюшной полости.
Современные методы проведения лечения
Чаще всего пациента госпитализируют с недугом, находящимся на стадии токсемии. Первичный диагноз лечащий врач устанавливает по характерным признакам. В дальнейшем диагноз требуется подтвердить или опровергнуть путем проведения инструментальной диагностики и лабораторных анализов.
Так как недуг способен развиваться непредсказуемо, то врач, занимающийся лечением, должен быть готов к развитию заболевания по любому сценарию. Лечебные мероприятия должны быть направлены на инактивирование ферментов, которые продуцируются поджелудочной. В процессе проведения лечебных мероприятий большое внимание следует уделить нормализации оттока секрета поджелудочной и очистке ее от образующихся токсичных соединений. Большое внимание в процессе лечения следует уделить купированию болевых ощущений.
Важно! Для пациента следует обеспечить голодание и полный эмоциональный покой.
 Наиболее информативным методом обследования является лапароскопия
Наиболее информативным методом обследования является лапароскопия
В процессе проведения лечебных процедур осуществляется промывание желудка при помощи холодной воды. Для этой цели используется зонд.
При осуществлении лечения проводится детоксикация. Это состояние достигается путем введения в организм мочегонных препаратов.
При правильном проведении лечебных процедур фаза токсемии завершается выздоровлением больного. В редких случаях она способна перерасти в фазу гнойных осложнений. При таком варианте течения болезни проводится хирургическое вмешательство, которое предполагает удаление пораженных участков органа.
Источник
Комментарии
Опубликовано в журнале:
“ХИРУРГИЯ” 9, 2017
М.А. Барская1, В.А. Завьялкин1, Д.В. Быков2, А.В. Варламов2, А.И. Кузьмин1, М.И. Терехина1, В.В. Щуклова1
1ФГБОУ «Самарский государственный медицинский университет Министерства здравоохранения Российской Федерации»; 2ГБУЗ СОКБ им. В.Д. Середавина, Самара, Россия
Ключевыеслова: деструктивныйпанкреатит, панкреонекроз, дети, реамберин.
Острый панкреатит у детей, являясь достаточно редкой патологией детского возраста [1—3], врачами первичного звена диагностируется лишь у 19,6% больных [4]. Причины острого панкреатита у детей многообразны. Часто эта патология развивается после травмы поджелудочной железы, в результате нарушения диеты, лекарственного воздействия [4—8].
По данным литературы, общая летальность при остром панкреатите в детском возрасте составляет 2,1%, а при деструктивных формах (панкреонекроз), являющихся тяжелым гнойно-септическим заболеванием, уровень смертности возрастает до 50% [4, 5, 7, 9].
Диагностика и лечение острого деструктивного панкреатита у детей является сложной проблемой. В лечебно-диагностическом алгоритме значительная роль принадлежит использованию таких методов, как компьютерная томография (КТ), прокальцитониновый тест (РСТ), диагностическая и лечебная лапароскопия, а также применение в комплексном лечении современных антибактериальных препаратов, ингибиторов протеаз (сандостатин) и экстракорпоральной детоксикации. Большое значение в терапии острого панкреатита приобретает инфузионная терапия, направленная на устранение нарушений обмена веществ на фоне эндогенной интоксикации, обеспечение транспорта кислорода к клеткам, а также поддержание оптимальных условий для его утилизации [10].
Любая гипоксия независимо от причин ее возникновения сопровождается повреждением дыхательной цепи митохондрий и энергодефицитом, поэтому даже при достаточном поступлении кислорода клетка не способна его использовать, что свидетельствует о необходимости введения дополнительных энергетических субстратов, способных восстановить функционирование дыхательной цепи митохондрий и поддержать жизнедеятельность клетки в целом.
Одним из инфузионых препаратов комплексного действия, обладающим выраженным цитопротекторным эффектом, является реамберин (ООО «НТФФ «ПОЛИСАН», Санкт-Петербург) — инфузионный антигипоксант на основе сукцината, что доказано в достаточно большом количестве исследований как у взрослых, так и у детей [10].
Цель исследования — изучение особенностей течения и результатов лечения острого деструктивного панкреатита у детей, лечившихся в детских хирургических отделениях Самары.
Материалиметоды
С 1999 по 2016 г. под нашим наблюдением в детских хирургических отделениях ЛПУ Самары находился 61 ребенок с различными формами панкреонекроза. В диагностике патологии применялись клинические, лабораторные, ультразвуковые методы исследования (УЗИ), компьютерная томография (КТ), диагностическая лапароскопия. Консервативное лечение острого панкреатита включало купирование болевого синдрома, подавление неукротимой рвоты, борьбу с парезом кишечника и нарушениями кислотно-щелочного равновесия, детоксика-цию, антиферментную и антибактериальную терапию. Пациенты были разделены на две группы: основную группу составили 17 пациентов, в программу инфузионной терапии которых входил антигипоксант реамберин в дозировке 10 мл на килограмм в сутки внутривенно, суточная доза распределялась на 2 введения в течение 5—7 дней. Контрольная группа состояла из 44 детей, у которых проводилась стандартная инфузионная терапия. Всем детям проводилась санация и сквозное дренирование полости сальниковой сумки трубчатым дренажем из ПВХ. У 53 (86,9%) пациентов в качестве доступа использовалась ла-паротомия, у 8 (13,1%) детей выполнено лапароскопическое вмешательство. Сквозные дренажи в послеоперационном периоде использовались для фракционного промывания сальниковой сумки, в дальнейшем через 7—14 дней (по уменьшению отделяемого детрита) дренаж менялся на леску, с последующем ее удалением через 1—1,5 мес. У 35 детей проводились наложение холецистостомы.
Распределениеразличныхформострогопанкреатитаввозрастномаспекте
| Форма панкреатита | 3—6 лет | 7—11 лет | 11—15 лет | Всего |
| Панкреонекроз жировой | 1 | 7 | 7 | 15 |
| Панкреонекроз геморрагический | 1 | 9 | 7 | 17 |
| Панкреонекроз смешанный | 1 | 8 | 20 | 29 |
Результатыиобсуждение
При панкреонекрозе выявлены следующие этиологические факторы:
- закрытая травма живота — 19 детей;
- открытая травма живота — 1;
- алиментарный фактор — 16;
- после операции по поводу ВПС (тетрады Фалло) — 1.
В 24 наблюдениях причина панкреонекроза не уста
новлена.
В работе использована классификация, предложенная на IХ Всероссийском съезде хирургов, основанная на известной классификации, принятой на международном съезде панкреатологов в Атланте в 1992 г.
Распределение пациентов по формам панкреонекро-за представлены в таблице.
Оперативные вмешательства выполнялись по следующим показаниям:
- перитонит;
- инфицированный панкреонекроз;
- аррозивное кровотечение;
- забрюшинная флегмона.
При панкреонекрозе отмечены следующие осложнения:
- ферментативный перитонит — 31;
- параколическая флегмона — 2;
- аррозивное кровотечение — 2;
- панкреатогенный абсцесс — 2;
- флегмона толстой кишки — 2;
- тяжелый сепсис с ПОН — 3.
Панкреонекроз у детей сопровождался выраженной
симптоматикой и тяжелым течением. Дети младшего возраста были беспокойными, отказывались от еды, появлялась рвота. Двигательное беспокойство сменялось адинамией, отсутствием реакции на окружающих. Старшие дети жаловались на боли в эпигастральной области, опоясывающую боль, иррадиацию боли в левую лопатку, левое надплечье, многократную рвоту, не приносящую облегчения. В рвотных массах в начале определялось желудочное содержимое, а затем — «застойное». Быстро развивались признаки интоксикации: головная боль, слабость, повышение температуры тела до субфебрильной или фебриль-ной, озноб, спутанность сознания, тахикардия, олигурия.
При клиническом исследовании определялось вздутие живота в эпигастрии, болезненность и напряжение в этой же области, положительный симптом Щеткина— Блюмберга, положительный симптом Воскресенского (исчезновение пульсации брюшной аорты), положительный симптом Мейо—Робсона (болезненность в реберно-позвоночном углу слева).
Прогрессирование панкреонекроза клинически выражалось в нарастании симптомов интоксикации, появлении гектической лихорадки.
Диагностика острого деструктивного панкреатита основывалась на детальной оценке клинической картины, лабораторных показателей, данных УЗИ, КТ, лапароскопии.
У всех больных с панкреонекрозом при поступлении отмечался гиперлейкоцитоз, увеличение ЛИИ, гипергликемия, повышение амилазы крови и мочи в 3—10 раз, значительное увеличение липазы в сыворотке крови, повышение С-реактивного белка до 150 мг/л, повышение РСТ больше 10. Ультразвуковое исследование позволяло выявить изменение эхогенности поджелудочной железы, выпот в сальниковой сумке и брюшной полости. При КТ выявлялись: изменение структуры поджелудочной железы, перипанкреатогенная инфильтрация, выпот в сальниковой сумке. У 2 (3,2%) больных с панкреонекрозом выявлены абсцессы железы.
Оперирован 61 пациент с панкреонекрозом. Хирургическая тактика заключалась в срединной лапаротомии (у 53 (86,9%) больных) или лапароскопии (у 8 (13,1%) пациентов), ревизии сальниковой сумки с осмотром поджелудочной железы, сквозном дренировании сальниковой сумки и дренировании брюшной полости. При наличии напряженного желчного пузыря производилась холеци-стостомия. У 4 (6,5%) больных во время оперативного вмешательства обнаружено вовлечение в воспалительный процесс брыжейки поперечной ободочной кишки. Этим пациентам выполнено дополнительное дренирование брюшной полости силиконовым перфорированным дренажем из свободной брюшной полости через mesocolon, сальниковую сумку с выведением дренажа через контрапертуру в левом подреберье. В 2 (3,2%) наблюдениях диагностирована флегмона ободочной кишки, произведена резекция толстой кишки с выведением терминальной илеостомы.
У 9 (14,8%) пациентов с посттравматическим деструктивным панкреатитом диагностировано повреждение селезенки. В 3 (4,9%) наблюдениях выполнена спленэкто-мия, у 6 (9,8%) больных произведены органосохраняющие операции (ушивание области повреждения с использованием ТахоКомба). Затем были выполнены сквозное дренирование сальниковой сумки и дренирование брюшной полости. Сквозные дренажи в послеоперационном периоде использовались для фракционного промывания сальниковой сумки.
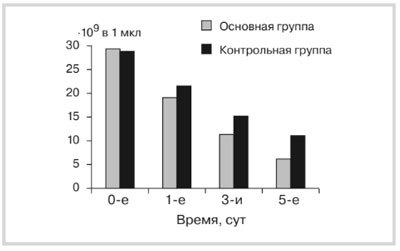
Рис. 1. Динамикалейкоцитозаудетейспанкреонекрозом.
Рис. 2. ДинамикаЛИИдетейспанкреонекрозом.
При уменьшении или исчезновении в промывных водах секрета поджелудочной железы и некротических масс сквозные трубчатые дренажи менялись на трубчатые дренажи меньшего диаметра, затем на леску, которая удалялась через 1—1,5 мес. Трубчатый дренаж из холецистосто-мы удаляли по мере уменьшения или исчезновения выделения желчи. Все пациенты с панкрео некрозом получали интенсивную терапию с применением тропных к ткани поджелудочной железы антибиотиков (карбапенемы, аминогликозиды, цефалоспорины III, IV поколений), сандостатин, местную гипертермию, инфузионную терапию, гипербарическую оксигенотерапию.
Изучение уровня лейкоцитов у детей с панкреонекро-зом при поступлении в стационар выявило его значимое увеличение во всех группах сравнения. Динамика лейкоцитоза обнаружила статистически достоверное снижение показателей на 3-и сутки у пациентов основной группы по сравнению с контрольной (p≤0,5). Изучение динамики уровня лейкоцитов показало статистически достоверное снижение этого показателя на 3-и сутки в основной группе пациентов (11,3·109±1,3) по сравнению с контрольной (15,5·109±1,2) при p=0,005 и на 5-е сутки в основной группе (до нормы: 7,6·109±0,9) по сравнению с контрольной (11,7·109±1,1) при p=0,001 (рис. 1).
Анализ динамики показателя лейкоцитарного индекса интоксикации по Кальф—Калифу у детей с панкреоне-крозом выявил статистически значимое увеличение в основной (до 3,2±0,2) и контрольной (3,3±0,4) группах, p≤0,5. Через 1 и 3 дня обнаружено более значимое достоверное снижение ЛИИ у пациентов основной группы (до 1,8±0,2, p=0,01 и 1,3±0,3 соответственно) по сравнению с детьми контрольной группы (до 2,5±0,3 и 1,7±0,2 соответственно). Через 5 дней результаты сравнения ЛИИ у больных основной группы достоверно подтвердили снижение данного показателя практически до нормы (1,07±0,2) в отличие от ЛИИ у детей контрольной группы (1,3±0,2) (p≤0,5) (рис. 2).
Изучение изменений СОЭ выявило через 1 и 3 дня значимое снижение данного показателя у детей основной группы до 12,3±1,2 и 9,7±0,9 мм/ч соответственно по сравнению с детьми контрольной группы (до 15,7±0,9 и 13,2±1,1 мм/ч соответственно), p≤0,5. Через 5 сут результаты анализа СОЭ выявили достоверное уменьшение практически до нормы у детей основной (6,3±0,3 мм/ч) и контрольной групп до 9,5±0,9 мм/ч, p=0,01.
Исследование динамики регрессии кишечной недостаточности кишечника обнаружило достоверно значимое ее купирование у пациентов основной группы уже на 2-е сутки по сравнению с контрольной группой, у которых нормализация данного показателя происходила на 3—5-е сутки, в среднем на полтора дня позже p≤0,5.
Анализ динамики показателей ферментов поджелудочной железы не выявил статистически значимых различий в основной и контрольной группах.
Среднее пребывание больных с панкреонекрозом составило 40,5 дня.
Умерли 3 (4,9%) детей с панкреонекрозом: 1 ребенок с забрюшинной флегмоной, тяжелым сепсисом с полиорганной недостаточностью; 2 (3,8%) детей с флегмоной толстой кишки, тяжелым сепсисом с полиорганной недостаточностью.
В 4 наблюдениях сформировались кисты поджелудочной железы, которые дренированы под контролем УЗИ. Дети выздоровели.
Заключение
Исследование сравнимых показателей основной и контрольной групп обнаруживают более быстрое снижение симптомов интоксикации, таких как лейкоцитоз, лейкоцитарной индекс интоксикации, исчезновение эн-теральной недостаточности, в инфузионной терапии которых применялся Реамберин.
Вывод
Несмотря на редкость острого панкреатита у детей, следует помнить о возможности развития деструктивного процесса в поджелудочной железе (панкреонекроза).
В этиологии острого панкреатита имеет значение закрытая травма живота, нарушение диеты, хронические заболевания ЖКТ, печени, желчного пузыря.
В диагностике деструктивного панкреатита наряду с клиникой большое значение имеют лабораторные данные, УЗИ, КТ, диагностическая лапароскопия.
При инфицированном панкреонекрозе необходимо адекватное дренирование и санация сальниковой сумки.
Применение в инфузионной терапии антигипоксанта реамберин позволяет быстрее добиться снижения симптомов интоксикации и, как следствие, уменьшить сроки пребывания больных с панкреонекрозом в стационаре.
Авторы заявляют об отсутствии конфликта интересов.
ЛИТЕРАТУРА/REFERENCES
1. Болезниподжелудочнойжелезыудетей. Под ред. Бельмера С.В., Разумовского А.Ю., Корниенко Е.А., Приворотского В.Ф. М.: Медпрактика-М; 2015. [Diseases of the pancreas in children. Eds. Bel’mer S.V., Razumovskogo A.Yu., Kornienko E.A., Приворотско-го V.F. M.: Medpraktika-M; 2015. (In Russ.).]
2. Гасилина Т.В., Бельмер С.В. Панкреатиты у детей. Лечащийврач. 2009;1. [Gasilina TV, Belmer SV. Pancreatitis in children. Lechashchii vrach. 2009;1. (In Russ.).]
3. Cofini M, Favoriti P, Quadrozzi F. Acute pancreatitis in pediatric age: our experience on 52 cases. Minerva Pediatr. 2014;66:4:275-280.
4. Цуман В.Г., Римарчук Г.В., Шербина В.И., Семилов Э.А., На-ливкин А.Е., Сивенкова Н.В. и др. Острыйпанкреатитудетей (клиника, диагностика, лечение). Пособие для врачей. Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского. 2001. [Tsuman VG, Rimarchuk GV, Sherbina VI, Semilov EA, Nalivkin AE, Sivenkova NV. Acute pancreatitis in children (clinic, diagnosis, treatment). Manual for doctors. And others — Moscow Regional Scientific Research Clinical Institute M.F. Vladimirsky. 2001. (In Russ.).]
5. Баиров Г.А. Хирургияподжелудочнойжелезыудетей. Л.: Медицина; 1978. [Bairov GA. Pancreas surgery in children. L.: Medicine; 1978. (In Russ.).]
6. Барская М.А., Быков Д.В., Варламов А.В., Завьялкин В.А., Кузьмин А.И., Бородин Р.В., Каганов И.Ю. Особенности клиники, диагностики и лечения деструктивного панкреатита у детей.
Международныйжурналприкладныхифундаментальныхисследований. 2015;12-17:1220-1222. [Barskaya MA, Bykov DV, Var-lamov AV, Zavyalkin VA, Kuzmin AI, Borodin RV, Kaganov I.Yu. Features of the clinic, diagnosis and treatment of destructive pancreatitis in children. Mezhdunarodnyi zhurnal prikladnykh i fundamental’nykh issledovanii. 2015;12-17:1220-1222. (In Russ.).]
7. Вашетко Р.В., Толстой А.Д., Курыгин А.А., Стойко Ю.М., Крас-ногоров В.Б. Острыйпанкреатититравмыподжелудочнойжелезы. Руководство для врачей. СПб.: Из-во «Питер»; 2000. [Vashko RV, Tolstoy AD, Kurygin AA, Stoiko YuM, Krasnogorov VB. Acute pancreatitis and pancreatic trauma: a guide for doctors. St. Petersburg: Publishing House «Peter»; 2000. (In Russ.).]
8. Kandula L, Lowe ME. Etiology and outcome of acute pancreatitis in infants and toddlers. J Pediatr. 2008;152:106-110.
9. Костюченко А.Л., Филин В.И. Неотложнаяпанкреатология. Справочник для врачей. Издание 2-е, исправ. и доп. СПб.: Из-во «Деан»; 2000. [Kostyuchenko AL, Filin VI. Emergency pancreatology. A reference book for doctors. Edition 2-rd, revised and enlarged. SPb.: Publishing house «Dean»; 2000. (In Russ.).]
10. Александрович Ю.С., Пшениснов К.В. Инфузионные антиги-поксанты при критических состояниях у детей. Общаяреаниматология. 2014;X(3):61-76. [Aleksandrovich YuS, Pshenisnov KV. Infusion antihypoxants in critical conditions in children. Obshchaya reanimatologiya. 2014;X(3):61-76. (In Russ.).]
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник
