Нестероидные противовоспалительные препараты и язва желудка
Что вы делаете, когда болит голова, поднялась высокая температура или беспокоит боль в суставах? 90% опрошенных ответят: «Пью таблетку».
«Волшебные» пилюли
Существует группа препаратов, под общим названием нестероидные противовоспалительные (НПВП), которые мы все хотя бы раз в жизни, а многие регулярно, принимали. Это препараты, обладающие обезболивающим противовоспалительным и / или жаропонижающим действием. В качестве примера можно назвать Аспирин, Нурофен, Найс, Кетанов, Кетопрофен и прочие. Учитывая «волшебные эффекты» от их действия — снятие воспаления, боли и жара, — их назначают практически все, всем и всегда. Назначают травматологи, ревматологи, терапевты, лоры, стоматологи. Плюс, их можно совершенно свободно приобрести в любой аптеке. Но, наряду с «волшебными свойствами» эти лекарства обладают рядом побочных действий, которые можно разделить на 2 группы: кардиориски и гастро риски. Собственно о гастрорисках и пойдёт речь в данной статье.
НПВП-гастропатия
В научной литературе эта проблема называется «НПВП-гастропатия». Впервые термин был предложен в 1986 году для разграничения специфического поражения слизистой оболочки желудка, возникающего при длительном употреблении НПВП, от классической язвенной болезни.
Отличие НПВП-гастропатии от язвенной болезни можно проследить и по зоне поражения. Чаще всего язвы можно увидеть в желудке, а не в 12-перстной кишке. Плюс, изменения встречаются чаще у пожилых, а не у молодых людей.
Немного цифр
Немного статистики. В Великобритании назначается около 24 млн. НПВС в год. 70% лиц старше 70 лет принимают НПВС 1 раз в неделю, а 34% ежедневно. В США продается НПВС на сумму до 6 млрд. в год. Как следствие, риск развития желудочно-кишечных кровотечений (ЖКК) возрастает 3–5 раз, прободения — в 6 раз, риск смерти от осложнений до 8 раз. До 40–50% всех случаев острых ЖКК связаны с НПВС.
Проблема эта актуальна и в нашей стране, к примеру по данным Научного Центра сердечно-сосудистой хирургии им. А.Н. Бакулева из 240 больных, ежедневно принимающих аспирин даже в малых дозах, на гастроскопии поражения желудка и 12 п.к выявлены у 30% (из них язвы — у 23,6%, эрозии — у 76,4%). Аналогичная картина у коллег из ВНИИ ревматологии РАМН — у 2126 пациентов, принимающих НПВС без «прикрытия» (защиты) желудка, эрозии и язвы гастродуоденальной зоны найдены в 33,8% случаев. Это очень впечатляющие и драматические цифры осложнений от приема НПВС, учитывая количество употребляющих эти препараты людей в развитых странах.
Как это работает?
Как же действуют эти препараты в наших желудках? Всё очень просто, негативное воздействие реализуется за счёт дисбаланса защитных и агрессивных сил. У нас в желудке существует ряд защитных механизмов, позволяющих противостоять натиску агрессоров. Среди последних:
- Кислота, которая по своему pH-балансу приближается к аккумуляторной кислоте
- Желчь и сок поджелудочной железы, которые могут забрасываться в желудок.
- Ряд лекарственных препаратов.
- Алкоголь и никотин.
- Раздражающие пищевые компоненты (специи, острая пища и т.д.)
- Инфекция Helicobacter pylori и так далее.
Защищается желудок за счет мощного слоя слизи и бикарбонатов, которые нейтрализуют кислоту, адекватного кровоснабжения, способности очень быстро регенерировать. Когда мы используем НПВС препараты, баланс сил изменяется в сторону агрессивных механизмов и происходит поражение слизистого и подслизистого слоя желудка и 12-перстной кишки.
Диагностика
Для диагностики подобных изменений используется гастроскопия, являющаяся «золотым стандартом». Интересный факт, дело в том, что порядка 40% больных с эрозивно-язвенными изменениями, принимающих эти препараты длительно (более 6 недель) не ощущают никакого дискомфорта или неприятных, болезненных ощущений. Проблемы с желудком диагностируются лишь при походе к другим врачам, а не к гастроэнтерологу. И, наоборот, у 40% пациентов, на фоне жалоб, которые они предъявляют, ничего не находят.
Что же делать в таком случае?!
Алгоритм действий для пациентов, не имеющих проблем с желудком, и тех, у кого в анамнезе была язвенная болезнь или эрозивные изменения, различен. Для первой группы, при назначении нестероидных противовоспалительных препаратов более, чем на 5 дней, обязательно назначение препаратов из группы ингибиторов протонной помпы (ИПП). Таких как, омепразол, пантопразол, рабепразол и т. д. (на весь курс приема). Для второй группы, любые назначения из группы НПВС, независимо от срока приёма, требуют параллельного назначения ингибиторов протонной помпы. Так же обязателен прием ИПП пациентам, принимающих длительно аспирин.
Мифы, с которыми мы сталкиваемся в ежедневной практике
Миф 1. Использование НПВС препаратов в виде свечей является менее агрессивным для желудка, нежели приём таблеток
Это 100% миф. Патогенное, разрушительное действие лекарства реализуется через кровь, доставляющую его по сосудам в желудок.
Миф 2. В качестве «гастропротекторов» можно использовать лекарства из группы антацидов — Ренни, Маалокс, Фосфалюгель и H2-блокаторы (Ранитидин и Фамотидин)
В данном случае они не эффективны.
Миф 3. Принимать ингибиторы протонной помпы можно нерегулярно
Дело в том, что если пожилому человеку назначили на всю жизнь противовоспалительный препарат, абсолютно бессмысленно назначать гастропротекцию на месяц. В подобных случаях лекарства должны приниматься строго параллельно.
Миф 4. В качестве «гастропротекторов» могут выступать пищевые продукты (кисели и пр.)
Этот миф, как абсолютно фантастический, мы оставим без комментариев.
Как выбрать лекарство
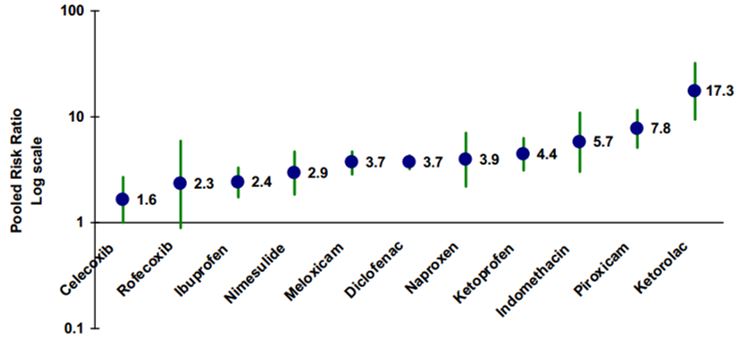
На самом деле, самым важным моментом является то, какие именно лекарства мы принимаем. На рисунке можно увидеть шкалу агрессивности различных препаратов из группы НПВС по отношению к желудку.
Самыми агрессивными препаратами являются Аспирин, Кеторолак, Пироксикам, Индометацин. По возможности рекомендуется использовать селективные препараты, которые обладают минимальными гастро-рисками. Их применение всегда более желательно, к ним относится Целекоксиб и Рофекоксиб. Но несмотря на их относительную безопасность, назначать их должен строго по показаниям лечащий доктор, не забывайте об этом.
Про Helicobacter pylori
Еще одним очень важным компонентом профилактики осложнений, является диагностика инфекции Helicobacter pylori у пациента планирующего длительно принимать НПВС (особенно аcпирин). Наличие бактерии увеличивает риски эрозивно-язвенных поражений ЖКТ и кровотечения в 2–3 раза. При её выявлении должна в обязательном порядке проводится эрадикация (уничтожение этой бактерии).
Резюме
Итак делаем выводы:
- Перед длительным приемом НПВС обязательным является сбор анамнеза для исключения патологий ЖКТ в прошлом, по необходимости проведение гастроскопии, диагностика и лечение хеликобактериоза.
- Выбирая, чем лечиться, по возможности следует останавливаться на селективных НПВС.
- При назначении неселективных НПВС более 5 дней и у пациентов с эрозивно-язвенными изменениями в анамнезе даже с селективными НПВС обязателен прием препаратов «прикрывающих» желудок (ИПП).
- Всем пациентам в возрастной группе после 60 лет, регулярно принимающим аспирин, обязательно проводить гастроскопию и при высоких рисках принимать постоянно препараты из группы ИПП.
- Прием гастроэнтеролога в нашей клинике – 3 900 рублей
Источник
На вопросы врачей отвечает доктор медицинских наук, профессор кафедры пропедевтики внутренних болезней 1 МГМУ имени И.М. Сеченова Аркадий Александрович Шептулин.
Почему, несмотря на наличие в настоящее время более безопасных НПВП и эффективных средств лекарственной профилактики, частота эрозивно-язвенных поражений при приеме НПВП не снижается?
Высокой частоте НПВП-ассоциированной гастропатии способствует целый ряд факторов. Прежде всего, это все возрастающая распространенность приема НПВП, обусловленная общей тенденцией к старению населения и, как следствие, увеличению больных с артрозами, остеохондрозом позвоночника и другими заболеваниями, требующими проведения терапии противовоспалительными препаратами и анальгетиками. Показано, например, что 70% лиц старше 65 лет в США принимают НПВП хотя бы 1 раз в неделю, 34% – ежедневно [1].
Кроме того, поскольку НПВП относятся к препаратам группы OTC (over-the-counter), т. е. безрецептурным лекарственным средствам, многие больные убеждены в их безопасности и не читают внимательно инструкций по их правильному применению [2].
Анальгетический эффект НПВП приводит к тому, что у больных могут отсутствовать боли и диспепсические симптомы, которые могли бы насторожить пациентов и указать на возможное неблагоприятное побочное действие препаратов, и тогда первым клиническим проявлением осложнений лекарственной терапии являются желудочно-кишечное кровотечение или прободение язв.
Наконец, многие больные вынуждены параллельно принимать другие препараты, например, малые дозы ацетилсалициловой кислоты (АСК), назначаемые кардиологами для профилактики осложнений ишемической болезни сердца, или препараты, тормозящие агрегационную способность тромбоцитов (клопидогрел), рекомендуемые в течение длительного времени после стентирования коронарных артерий, которые в комбинации с НПВП значительно повышают риск развития НПВП-гастропатии.
Какие факторы повышают риск развития эрозивно-язвенных поражений желудка и двенадцатиперстной кишки при приеме НПВП?
Главными из них являются наличие в анамнезе осложнений язвенной болезни (ЯБ) (относительный риск (ОР)=13,5), одновременный прием нескольких НПВП (ОР=9,0), высокие дозы НПВП (ОР=7,0), одновременный прием антикоагулянтов (ОР=6,4), наличие в анамнезе неосложненной ЯБ (ОР=6,1), возраст старше 70 лет (ОР=5,6), одновременный прием кортикостероидов (ОР=2,2) (рис. 1).
Дополнительными факторами риска возникновения НПВП-гастропатии служат продолжительность лечения (наибольшая вероятность развития гастродуоденальных эрозий и язв отмечается в 1-й мес. приема НПВП, затем она несколько снижается и стабилизируется после 4-го мес. лечения), курение (особенно в сочетании с указанием на наличие в анамнезе ЯБ) и злоупотребление алкоголем, применение данных препаратов перед едой, а не после приема пищи, наличие предшествующих и сопутствующих заболеваний, таких как гастроэзофагеальная рефлюксная болезнь, стриктуры пищевода, системная склеродермия с поражением пищевода и желудка, цирроз печени (особенно осложнившийся портальной гастропатией), заболевания сердечно-сосудистой системы, хроническая почечная недостаточность [3–6].
Какова роль инфекции Helicobacter pylori (НР) в развитии НПВП-гастропатии?
До недавнего времени этот вопрос освещался в литературе противоречиво. В ряде работ указывалось, что сопутствующая инфекция НР повышает риск развития НПВП-гастропатии в 1,5–1,8 раза. Но были и противоположные мнения, согласно которым наличие этой инфекции способствует более быстрому заживлению эрозий и язв желудка и двенадцатиперстной кишки, вызванных приемом НПВП. В настоящее время, согласно заключению последнего согласительного совещания Европейской рабочей группы по изучению НР «Маастрихт-4», инфекция HР рассматривается как независимый фактор риска развития гастродуоденальных язв и их осложнений при приеме НПВП [7].
Почему у женщин эрозивно-язвенные поражения желудка и двенадцатиперстной кишки встречаются чаще, чем у мужчин?
Пол сам по себе не является фактором, влияющим на риск развития НПВП-гастропатии. Ее несколько более высокая частота у женщин объясняется просто более частым применением женщинами препаратов данной группы (например, по поводу головных болей, болей в животе, связанных с менструальным циклом и т. д.).
Какие НПВП обладают наиболее выраженным неблагоприятным влиянием на слизистую оболочку желудка и двенадцатиперстной кишки?
Был проведен метаанализ работ, посвященных изучению ульцерогенных свойств различных НПВП, который свидетельствовал о том, что ОР развития гастродуоденальных эрозивно-язвенных поражений при их приеме неодинаков. Если принять ОР возникновения эрозий и язв желудка и двенадцатиперстной кишки при приеме ибупрофена – препарата с наименьшим риском развития НПВП-ассоциированной гастропатии – за 1,0, то для диклофенака он составит 2,3, для АСК – 4,8, для индометацина – 8,0, для пироксикама – 9,0, для кетопрофена – 10,3 [8]. Сходные результаты были получены и в других исследованиях. Так, анализ банка данных 17 центров США и Канады, насчитывающего 36 тыс. больных с ревматическими заболеваниями, показал, что наименьшей ульцерогенностью среди НПВП обладают ибупрофен и салицилаты, наибольшей – индометацин и кетопрофен [9].
Снижается ли риск возникновения НПВП-гастропатии при применении парентеральных форм НПВП, использовании быстрорастворимых форм АСК, лекарственных форм с энтеральным покрытием?
В свое время на совершенствование лекарственных форм НПВП или изменение пути их введения возлагались определенные надежды в плане снижения их ульцерогенного действия. Однако оказалось, что достаточно высокий риск возникновения гастродуоденальных эрозивно-язвенных поражений верхних отделов ЖКТ сохраняется и при применении быстрорастворимых форм АСК, а также при использовании препаратов с энтеральным покрытием [10]. Вообще, как подчеркивалось в специальном сообщении Информационной программы по здравоохранению, посвященном безопасности применения безрецептурных анальгетиков в США, обилие на фармацевтическом рынке различных НПВП не должно создавать ложного впечатления их безопасности в отношении возможного развития осложнений со стороны ЖКТ [11].
Насколько эффективно снижают селективные НПВП риск развития эрозивно-язвенных поражений желудка и двенадцатиперстной кишки?
Как известно, неодинаковая ульцерогенность различных НПВП связана с разным соотношением ингибирующих эффектов применительно к активности фермента циклооксигеназы-1 (ЦОГ-1), отвечающей за цитопротективные свойства слизистой оболочки желудка и двенадцатиперстной кишки, и циклооксигеназы-2 (ЦОГ-2), участвующей в реализации воспалительных реакций. Были синтезированы новые НПВП, обладающие слабым ингибирующим действием в отношении активности ЦОГ-1 (мелоксикам, нимесулид) или же селективно подавляющие активность ЦОГ-2 (целекоксиб, рофекоксиб).
Применение этих препаратов, действительно, несколько снижает частоту возникновения НПВП-гастропатии, однако риск развития гастродуоденальных эрозивно-язвенных поражений при их назначении все равно сохраняется (рис. 2). Так, если при приеме неселективных НПВП ОР возникновения осложнений со стороны верхних отделов ЖКТ составлял 1,77, то при применении селективных НПВП (нимесулид, мелоксикам, коксибы) – 1,30–1,33 [12].
Был проведен метаанализ 26 исследований, сравнивавших способность коксибов уменьшать риск возникновения диспепсических жалоб по сравнению с традиционными НПВП, а также по сравнению с применением комбинации традиционных НПВП и ингибиторов протонной помпы (ИПП). Оказалось, что коксибы снижали ОР возникновения симптомов диспепсии лишь на 12%, тогда как применение традиционных НПВП с комбинации с ИПП уменьшало этот риск на 66% [13] (рис. 3).
В 2004 г. рофекоксиб был отозван с фармацевтического рынка из-за доказанного повышения частоты инфаркта миокарда у больных, получавших данный препарат с целью профилактики рецидива колоректального рака. В настоящее время признано нежелательным назначение коксибов пожилым больным с высоким риском развития кардиоваскулярных осложнений [14].
Какие препараты в настоящее время являются наиболее предпочтительными для лечения НПВП-ассоциированной гастропатии?
В лечении НПВП-ассоциированной гастропатии в настоящее время применяются препараты трех групп: синтетические аналоги простагландина Е1 (мизопростол), блокаторы Н2-рецепторов гистамина и ИПП. Проведенные многоцентровые рандомизированные контролируемые сравнительные исследования подтвердили более высокую эффективность ИПП.
Алгоритм лечения НПВП-ассоциированной гастропатии предполагает прежде всего решение вопроса о возможности отмены АСК и других неселективных НПВП и замены их другими анальгетиками (парацетамол) или селективными ингибиторами ЦОГ-2. Если таковая возможность имеется, то после перевода больных на прием селективных ингибиторов ЦОГ-2 назначаются (сроком на 4–8 нед.) ИПП в стандартных суточных дозировках: омепразол – в дозе 20 мг, пантопразол (Нольпаза) – 40 мг, рабепразол – 20 мг, эзомепразол – 20 мг. При осложненном течении эрозий и язв данные препараты применяются в двойных дозах. Н2-блокаторы и мизопростол в этих случаях менее эффективны, чем ИПП. Кроме того, недостатками мизопростола являются системный характер его действия и высокая частота развития диареи.
При невозможности отмены АСК и неселективных НПВП лечение гастродуоденальных эрозивно-язвенных поражений осуществляется на фоне их продолжающегося приема, но предпочтительнее с применением удвоенных доз ИПП. После заживления эрозий и язв назначается постоянная поддерживающая терапия стандартными дозами ИПП на весь период приема НПВП [15, 16].
Назначение каких ИПП является в настоящее время наиболее предпочтительным при лечении НПВП-ассоциированной гастропатии?
Различные ИПП сходны между собой по механизму действия, и как класс лекарственных препаратов по многим важным параметрам (выраженность антисекреторного эффекта, продолжительность действия) значительно превосходят блокаторы Н2-рецепторов гистамина. Однако между самими ИПП существуют значительные различия, связанные с особенностями фармакокинетики и фармакодинамики.
Период полураспада различных ИПП оказывается неодинаковым. Для лансопразола он составляет 15 ч, для омепразола и рабепразола – менее 30 ч, для пантопразола – 46 ч. Эти различия обусловливаются особенностями взаимодействия данных ИПП с ферментом Н+, К+-АТФазой. Для нормального функционирования этого фермента важны 2 цистеиновых остатка, которые находятся в позициях 813 и 822. Связывание хотя бы с одним из цистеиновых остатков ведет к ингибированию протонной помпы. И омепразол, и пантопразол связываются с цистеином 813, но только пантопразол взаимодействует с цистеином 822 глубоко в мембране париетальной клетки. При этом связывание пантопразола с Н+, К+–АТФазой (в отличие от других ИПП) является необратимым, что определяет б|ольшую продолжительность антисекреторного действия пантопразола [17].
Кроме того, как известно, ИПП метаболизируются в печени системой цитохрома Р450, которая участвует в метаболизме и других лекарственных препаратов. При применении омепразола это может привести к нежелательным лекарственным взаимодействиям в случае одновременного приема таких лекарственных препаратов, как диазепам, варфарин, фенитоин и др. Пантопразол обладает самым низким среди всех ИПП сродством к системе цитохрома Р450, что объясняется наличием у него альтернативного пути метаболизма с помощью сульфотрансферазы цитозоля. Это преимущество пантопразола может стать очень важным у пожилых больных, которые часто бывают вынуждены принимать большое число различных препаратов [18].
Клинические исследования подтвердили высокую эффективность пантопразола в лечении эрозий и язв желудка и двенадцатиперстной кишки, вызванных приемом НПВП, в т. ч. и в тех случаях, когда больным нельзя было отменить прием указанных препаратов [19, 20]. При этом недавно проведенные исследования подтвердили безопасность пантопразола при его длительном применении (до 15 лет), не вызывавшем никаких клинически значимых изменений слизистой оболочки желудка [21].
Нужно ли у больных с НПВП-ассоциированной гастропатией проводить исследование наличия инфекции НР и последующую эрадикацию в случае ее обнаружения?
Согласно рекомендациям согласительного совещания «Маастрихт-IV», инфекция НР повышает риск развития НПВП-ассоциированной гастропатии, поэтому перед началом лечения данными препаратами необходимо обследование больных на наличие инфекции НР и проведение эрадикации в случае ее обнаружения [22]. Для диагностики инфекции НР используют быстрый (эндоскопический) уреазный тест, дыхательный уреазный тест, морфологический метод, определение антигена НР в кале, серологический метод.
Схемой первой линии в России является стандартная тройная схема эрадикационной терапии, включающая в себя ИПП (в стандартной дозе 2 р./сут), кларитромицин (по 500 мг 2 р./сут), амоксициллин (1000 мг 2 р./сут). С целью повышения ее эффективности рекомендуются назначение 2 р./сут повышенной дозы ИПП (удвоенной по сравнению со стандартной), увеличение продолжительности тройной терапии с ИПП и кларитромицином с 7 до 10–14 дней, добавление к стандартной тройной терапии висмута трикалия дицитрата в дозе 240 мг 2 р./сут, добавление к стандартной тройной терапии пробиотика Saccharomyces boulardii (энтерол по 250 мг 2 р./сут). Важно добиться точного соблюдения больными назначенного режима приема лекарственных средств.
Как вариант эрадикационной терапии первой линии (например, при непереносимости пенициллина) может быть назначена классическая четырехкомпонентная схема на основе висмута трикалия дицитрата (120 мг 4 р./сут) в комбинации с ИПП (в стандартной дозе 2 р./сут), тетрациклином (500 мг 4 р./ сут), метронидазолом (по 500 мг 3 р./сут) в течение 10 дней.
Квадротерапия с висмута трикалия дицитратом применяется также как основная схема терапии второй линии при неэффективности стандартной тройной терапии. Другой схемой терапии второй линии служит эрадикационная схема, включающая в себя ИПП (в стандартной дозе 2 р./сут), левофлоксацин (500 мг 2 р./сут) и амоксициллин (1000 мг 2 р./сут).
Как альтернативные варианты терапии первой линии предложены также последовательная терапия и квадротерапия без препаратов висмута.
При последовательной терапии больной получает первые 5 дней ИПП (в стандартной дозе 2 р./сут) в комбинации с амоксициллином (1000 мг 2 р./сут), а в последующие 5 дней – ИПП (в стандартной дозе 2 р./сут) в комбинации с кларитромицином (500 мг 2 р./сут) и метронидазолом (500 мг 2 р./сут).
Квадротерапия без препаратов висмута включает в себя ИПП (в стандартной дозе 2 р./сут), амоксициллин (1000 мг 2 р./сут), кларитромицин (500 мг 2 р./сут) и метронидазол (500 мг 2 р./сут). Оба альтернативных варианта эрадикационной терапии применяются и в случаях устойчивости штаммов НР к кларитромицину, однако в России эффективность этих схем не изучалась, что делает необходимым проведение собственных исследований.
Терапия третьей линии основывается на определении индивидуальной чувствительности НР к антибиотикам [23].
Всем ли больным, получающим НПВП, нужно проводить профилактику НПВП-ассоциированной гастропатии?
В настоящее время разработан определенный алгоритм профилактики НПВП-ассоциированной гастропатии, который определяет тактику врача в зависимости от риска возникновения эрозивно-язвенных поражений желудка и двенадцатиперстной кишки у данного конкретного пациента [24–27].
Низкий риск возникновения НПВП-гастропатии предполагает отсутствие у больного основных факторов риска (возраст старше 70 лет, терапия высокими дозами НПВП, наличие в анамнезе осложнений язвенной болезни, одновременный прием АСК даже в малых дозах, а также других НПВП, антикоагулянтов или кортикостероидов). В таких случаях профилактические мероприятия сводятся к назначению наименее ульцерогенных неселективных НПВП (например, ибупрофена), причем, по возможности, не в полной (2,4 г/сут), а в минимально эффективной суточной дозе.
Наличие у больного 1–2 факторов риска из приведенной выше группы позволяет оценить риск возникновения НПВП-гастропатии как средний (умеренный). Таким больным к перечисленным выше мерам добавляют антисекреторные препараты или мизопростол, либо прибегают к назначению селективных ЦОГ-2. При этом применение ИПП признано более предпочтительным, чем назначение Н2-блокаторов. Поскольку прием мизопростола в полной дозе (800 мкг) нередко сопровождается появлением диареи и схваткообразных болей в животе, то его дозу целесообразно снизить до 600 мкг/сут.
При обнаружении у больного комбинации таких факторов риска, как пожилой возраст, терапия высокими дозами НПВП, одновременный прием АСК, кортикостероидов или антикоагулянтов, риск развития эрозивно-язвенных поражений желудка и двенадцатиперстной кишки расценивается как высокий. Таким пациентам назначают ингибиторы ЦОГ-2 в комбинации с ИПП или мизопростолом.
Наконец, при очень высоком риске возникновения НПВП-гастропатии (наличие многих факторов риска и анамнестических осложнений язвенных поражений) следует, по возможности, отказаться от назначения НПВП. Если это сделать не удается, то необходимо отдавать предпочтение применению селективных ЦОГ-2 в комбинации с ИПП и/или мизопростолом [24–27].
Источник
